题目内容
【题目】写出下列反应的化学方程式或离子方程式。
(1)H2O2将碱性工业废水中的CN-氧化为碳酸盐和氨气的离子方程式:____________。
(2)硫化氢具有还原性,可以和许多氧化剂反应。在硫酸溶液中,H2S和KMnO4反应生成S、MnSO4、K2SO4和 H2O,写出该反应的化学方程式:________。
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2,写出该反应的离子方程式:__。
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:____。
(5)催化反硝化法中,H2能将![]() 还原为N2,反应进行一段时间后溶液呈碱性,写出该反应的离子方程式:________。
还原为N2,反应进行一段时间后溶液呈碱性,写出该反应的离子方程式:________。
【答案】H2O2+CN-+OH-= ![]() +NH3↑ 5H2S+2KMnO4+3H2SO4=5S↓+2MnSO4+K2SO4+8H2O Cl2+2
+NH3↑ 5H2S+2KMnO4+3H2SO4=5S↓+2MnSO4+K2SO4+8H2O Cl2+2![]() =2ClO2+2Cl- 2Fe3++3ClO-+10OH+=2
=2ClO2+2Cl- 2Fe3++3ClO-+10OH+=2![]() +3Cl-+5H2O 5H2+2
+3Cl-+5H2O 5H2+2![]() =N2+2OH-+4H2O
=N2+2OH-+4H2O
【解析】
(1)H2O2将碱性工业废水中的CNˉ氧化为碳酸盐和氨气,相应的离子方程式为:H2O2+CN-+OH-=CO32-+NH3↑;
(2)H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,结合原子守恒书写化学方程式,3H2SO4+5H2S+2KMnO4=5S↓+2MnSO4+K2SO4+8H2O;
(3)Cl2氧化NaClO2溶液制取ClO2,本身被还原为氯离子,1个氯气分子反应得到2个电子,因此离子方程式:Cl2+2![]() =2ClO2+2Cl- ;
=2ClO2+2Cl- ;
(4)FeCl3与KClO在强碱性条件下反应可制取K2FeO4,结合电子守恒、原子守恒和电荷守恒配平书写离子方程式:2Fe3++10OH-+3ClO-═2FeO42-+3Cl-+5H2O;
(5)催化反硝化法中,H2能将NO3-还原为N2,反应进行一段时间后溶液呈碱性,所以产生氢氧根离子,离子反应方程式为:2NO3-+5H2=N2+2OH-+4H2O。

 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】下列实验能达到预期目的是
编号 | 实验内容 | 实验目的 |
A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
B | 室温下,用pH试纸测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
C | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快 | 证明HX酸性比HY强 |
D | 向10mL 0.2mol/L NaOH溶液中滴2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下Ksp: Mg(OH)2>Fe(OH)3 |
A. AB. BC. CD. D
【题目】按要求回答下列问题
(1)我国规定生活用水中镉排放的最大允许浓度为0.005 mg/L。处理含镉废水可采用化学沉淀法。试回答下列问题:
①磷酸镉(Cd3(PO4)2)沉淀溶解平衡常数的表达式Ksp=_____________________。
②在某含镉废水中加人Na2S,当S2-浓度达到7.9 × 10-8mol/L时,水体中Cd2+浓度为_____mol/L(已知:Ksp(CdS)=7.9 × 10-27,Cd的相对原子质量:112);此时是否符合水源标准?______(填“是”或“否”)。
(2)炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:
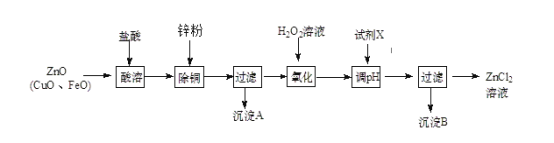
下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子 | Fe3+ | Zn2+ | Fe2+ |
开始沉淀的pH | 1. 1 | 5. 2 | 5. 8 |
沉淀完全的pH | 3. 2 | 6. 4 | 8. 8 |
①加入H2O2溶液的作用是________________。
②流程图中,调节pH时,加入的试剂X可以是________(填序号);
a、ZnO b、NaOH c、Zn2(OH)2CO3 d、ZnSO4
pH应调整到______________________。