题目内容
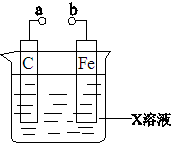
对下列装置的叙述错误的是

A.X如果是HCl,则不论a和b用导线连接还是a和b分别连接直流电源正、负极时,H+的移动方向均相同
B.X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加
C.X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应
D.X如果是NaCl,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程
【答案】
A
【解析】
试题分析:A、X如果是HCl, a和b用导线连接,则构成原电池,碳棒是正极,铁是负极。溶液中的氢离子向正极碳棒移动。如果a和b分别连接直流电源正、负极,则构成电解池,碳棒是阳极,铁是阴极,溶液中的H+向阴极铁移动,A不正确;B、X如果是硫酸铜,a和b分别连接直流电源正、负极,则构成电解池,碳棒是阳极,铁是阴极。铜离子在阴极得到电子,生成铜而析出,所以一段时间后铁片质量增加B正确;C、X如果是硫酸铁, a和b用导线连接,则构成原电池,碳棒是正极,铁是负极,铁失去电子,发生氧化反应。如果a和b不用导线连接,则铁和硫酸铁直接发生氧化反应,生成硫酸亚铁,因此铁发生氧化反应,C正确;D、X如果是NaCl,则a和b连接时构成原电池,碳棒是正极,铁是负极,失去电子,被腐蚀。所以该装置可模拟生铁在食盐水中被腐蚀的过程,D正确,答案选A。
考点:考查电化学原理的有关应用和判断

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目