题目内容
下列物质中都含有氢元素,按照已学知识判断其中属于酸的是
| A.NH3 | B.CH4 | C.NaHCO3 | D.HClO3 |
D
解析试题分析:电离的阳离子全部是氢离子的是算,故
考点:考查酸的定义。

练习册系列答案
相关题目
水溶液X中只可能溶有K+、Mg2+、Al3+、[Al(OH)4]-、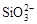 、
、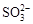 、
、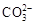 、
、 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验: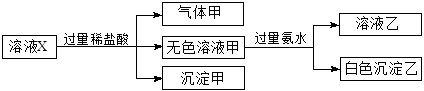
下列判断正确的是( )
| A.气体甲一定是纯净物 |
B.K+、[Al(OH)4]-和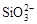 一定存在于溶液X中 一定存在于溶液X中 |
| C.沉淀甲是硅酸和硅酸镁的混合物 |
D.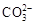 和 和 一定不存在于溶液X中 一定不存在于溶液X中 |
常温下,下列各组离子在指定溶液中一定能大量共存的是:
| A.能使淀粉-KI试纸显蓝色的溶液中:K+ SO42- S2- SO32- |
| B.含有0.1mol·L-1 Fe2+的溶液:Na+Cl- ClO- SO42- |
| C.c(H+)/c(OH-)=1012的溶液中:Al3+ NH4+ NO3- K+ |
| D.含有0.1mol·L-1 HCO3-的溶液:Na+ Fe3+ NO3- C6H5O- |
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )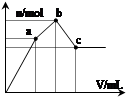
| A.a点的溶液呈中性 |
| B.b点到c点之间发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH— =Al(OH)3↓+2BaSO4↓ |
| C.c点加入Ba(OH)2溶液的体积为200 mL |
| D.c点溶液呈碱性 |
在由水电离出的c(H+)= 1×10-13 mol/L的溶液中,一定可以大量共存的是( )
| A.Ba2+ Na+ NO3- Cl- | B.Fe2+ Na+ NO3- Cl- |
| C.SO42- S2O2- 3 NH4+ Na+ | D.Mg2+ Na+ Br- AlO2- |
下列叙述正确的是( )
| A.固态氯化钾不导电,所以氯化钾不是电解质 |
| B.石墨能导电,所以石墨是电解质 |
| C.硫酸溶液能导电,所以硫酸是电解质 |
| D.CO2溶于水能导电,所以CO2是电解质 |
在下列各溶液中,离子一定能大量共存的是( )
| A.强碱性溶液中:K+、Al3+、Cl-、SO42- |
B.含有0.1 mol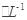 Fe3+的溶液中:K+、Mg2+、I-、NO3- Fe3+的溶液中:K+、Mg2+、I-、NO3- |
C.含有0.1mol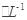 Ca2+溶液在中:Na+、K+、CO32-、Cl- Ca2+溶液在中:Na+、K+、CO32-、Cl- |
| D.室温下,pH=l的溶液中:Na+、Fe3+、NO3-、SO42- |
某溶液与过量的NH4HCO3溶液混合加热,既有气体生成,又有沉淀生成,则此溶液可能大量共存的离子组是 ( )
| A.K+ Cl- SO42- Ba2+ H+ | B.Mg2+ NO3- SO42- OH-Na+ |
| C.Mg2+ Na+ Cl- H+ NO3- | D.Na+ Ba2+ NO3- OH- Cl- |
下列各组离子一定能在无色溶液中大量共存的是
| A.Na+、CO32-、NO3-、AlO2- | B.K+、H+、CrO42-、SO32- |
| C.Al3+、Ba2+、HCO3-、Cl- | D.Fe3+、Mg2+、SCN-、Cl- |