题目内容
【题目】下列关于0.10 mol·L-1 NaHCO3溶液的说法正确的是( )
A. 溶质的电离方程式为NaHCO3===Na++H++CO![]()
B. 25 ℃时,加水稀释后,n(H+)与n(OH-)的乘积变大
C. 离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO![]() )+c(CO
)+c(CO![]() )
)
D. 温度升高,c(HCO![]() )增大
)增大
【答案】B
【解析】试题分析:A.NaHCO3为强电解质,溶质的电离方程式为NaHCO3═Na++HCO3-,故A错误;B.25℃时,加水稀释后,促进HCO3-水解,n(OH-)增大,c(OH-)减小,由Kw不变,可知c(H+)增大,则n(H+)增大,则n(H+)与n(OH-)的乘积变大,故B正确;C.由电荷守恒可知,离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故C错误;D.HCO3-水解为吸热反应,升高温度,促进水解,则c(HCO3-)减小,故D错误;故选B。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
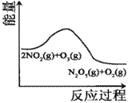
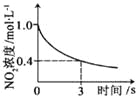
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B | C | D |
|
|
|
|
升高温度, | 0~3s内,反应速率为: | t1时仅加入催化剂, | 达平衡时,仅改变x,则x为c(O2) |