题目内容
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:归纳正确的是
①对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的产量一定增加
②常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合后形成溶液a,等浓度的盐酸与NaOH溶液等体积混合后形成溶液b,水的电离程度a>b。
③常温下,AgCl在同物质的量浓度的氨水和NaCl溶液中的溶解度比较,前者大。
④若将适量CO2通入0.1 mol/LNa2CO3溶液中至溶液恰好呈中性,则溶液中(不考虑溶液体积变化) 2c(CO32-)+ c(HCO3ˉ)= 0.1 mol/L
⑤常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则有:Ka·Kh=Kw
A.①②④⑤B.②④⑤C.②⑤D.①③⑤
【答案】D
【解析】
①化学平衡向正反应方向移动时,生成物的产量一定增加,正确;
②醋酸是弱酸,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合后,醋酸过量,溶液显酸性,抑制水的电离;等浓度的盐酸与NaOH溶液等体积混合后恰好反应生成氯化钠,对水的电离无影响,水的电离程度a<b,错误;
③常温下,AgCl在同物质的量浓度的氨水中反应生成二氨合银离子,溶解度较大,在NaCl溶液中,氯离子浓度增大,使氯化银的溶解平衡向左移动,溶解度减小,正确;
④将适量CO2通入0.1 mol/LNa2CO3溶液中至溶液恰好呈中性,溶液中的氢离子浓度等于氢氧根离子浓度,根据电荷守恒,2c(CO32-)+ c(HCO3ˉ)=c(Na+)=0.2mol/L,错误;
⑤醋酸的电离方程式为CH3COOH![]() CH3COO-+H+,醋酸电离平衡常数为Ka=
CH3COO-+H+,醋酸电离平衡常数为Ka=![]() ;醋酸根水解平衡常数为Kh=
;醋酸根水解平衡常数为Kh=![]() ;则Ka·Kh=
;则Ka·Kh=![]() ×
×![]() = c(H+)×c(OH-)=Kw,正确;
= c(H+)×c(OH-)=Kw,正确;
正确的有①③⑤,故选D。

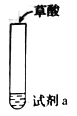
【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O