题目内容
【题目】取三份浓度均为0.1 mol/L,体积均为1 L 的CH3COONa 溶液中分别加入NH4Cl 固体、CH3COONH4固体、HCl 气体后所得溶液pH 变化曲线如图(溶液体积变化忽略不计)下列说法不正确的是
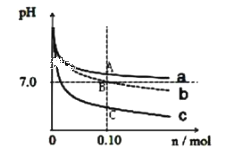
A.曲线 a、b、c 分别代表加入 CH3COONH4、NH4Cl、HCl
B.由图可知 Ka(CH3COOH)=Kb(NH3﹒H2O)=1×10-7
C.A点处 c(CH3COO-)>c(Na+)> c(NH4+)> c(OH-)> c(H+)
D.C点处 c(CH3COO-)+c(Cl-)+c(OH-)>0.1mol/L
【答案】B
【解析】
醋酸钠为强碱弱酸盐,因醋酸根离子水解,溶液呈碱性。往溶液中加入氯化铵固体,由于铵根离子水解呈酸性,故随着氯化铵的加入,溶液将由碱性逐渐变为酸性,由于水解微弱,所得溶液酸性较弱,符合的曲线为b;往溶液中通入氢化氯气体,随着气体的通入溶液由碱性转变为酸性,由于氯化氢为强酸,通入量较大时,溶液的酸性较强,符合的曲线为c;加入醋酸铵固体所对应的变化曲线为a,据此结合电荷守恒及盐的水解原理分析。
A.根据分析可知,曲线a代表醋酸铵、曲线b代表氯化铵、曲线c代表氯化氢,故A正确;
B.当加入固体的物质的量为0.1mol时,曲线b对应的pH值等于7,说明等浓度的醋酸根离子的水解程度与铵根离子相同,即Ka(CH3COOH)=Kb(NH3﹒H2O),但无法计算其电离平衡常数,故B错误;
C.A点含有的溶质为0.1molCH3COONa与0.1molCH3COONH4,溶液的pH>7,则c(OH)>c(H+),醋酸根离子的水解程度较小,则c(CH3COO)>c(Na+),铵根离子部分水解,则c(Na+)>c(NH4+),溶液中离子浓度的大小关系为:c(CH3COO-)>c(Na+)> c(NH4+)> c(OH-)> c(H+),故C正确;
D.C点通入0.1molHCl,与0.1mol醋酸钠反应得到0.1molCH3COOH与0.1molNaCl,c(Cl)=c(Na+)=0.1mol/L,则c(CH3COO)+c(Cl)+c(OH)>0.1mol/L,故D正确;
故选:B。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
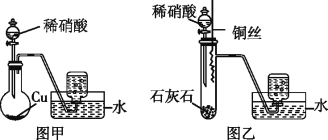
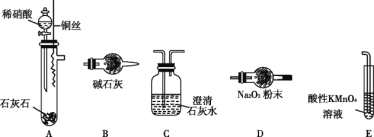
黄冈经典趣味课堂系列答案【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 稀硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
A.AB.BC.CD.D