题目内容
3.铬是人体必需的微量元素,它与脂类代谢有密切联系,能增强人体内胆固醇的分解和排泄,但铬过量会引起污染,危害人类健康.不同价态的铬毒性不同,三价铬对人体几乎无毒,六价铬的毒性为三价铬的100倍.下列叙述错误的是( )| A. | 在反应Cr2O72-+I一+H+→Cr3++I2+H2O中,氧化产物与还原产物的物质的量之比为3:2 | |
| B. | 一般情况下污水中的Cr3+在溶解的氧气的作用下易被氧化为Cr2O72- | |
| C. | K2Cr2O7可以氧化乙醇,该反应可用于检查酒后驾驶 | |
| D. | 维生素C具有还原性,发生铬中毒时,可服用维生素C缓解毒性 |
分析 A、化合价降低元素所在产物是还原产物,化合价升高元素所在产物是氧化产物;
B、Cr3+不能被氧气氧化;
C、K2Cr2O7可以氧化乙醇,产物呈紫色;
D、使六价铬变为三价铬,需要加入还原剂才能实现.
解答 解:A、在反应Cr2O72-+I-+H+→Cr3++I2+H2O中,根据电子守恒配平为:Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O,氧化产物是碘单质,还原产物是三价铬离子,二者的物质的量之比为3:2,故A正确;
B、氧气的氧化性较弱,Cr3+在溶解的氧气的作用下不能被氧化为Cr2O72-,故B错误;
C、K2Cr2O7可以氧化乙醇,产物呈紫色,该反应可用于检查酒后驾驶,故C正确;
D、发生铬中毒时,解毒原理是将六价铬变为三价铬,需要加入还原剂才能实现,可服用具有还原性的维生素C缓解毒性,故D正确.
故选B.
点评 本题考查学生氧化还原反应的综合知识,要求学生具有分析和解决问题的能力,有一定的难度,注意根据元素化合价的变化来分析.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
13.向含有ag硝酸的稀溶液中,加入bg铁粉充分反应,铁粉全部溶解.已知有$\frac{a}{4}$g硝酸被还原,则a:b不可能是( )
| A. | 3:1 | B. | 9:2 | C. | 2:1 | D. | 4:1 |
11.NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 常温常压下,11.2L一氧化碳分子数是0.5NA | |
| B. | NA个氧气分子和NA个氮气分子的质量比为7:8 | |
| C. | 常温常压下,2.86gNa2CO3•10H2O含有的Na+数为0.02NA | |
| D. | 物质的量浓度为0.5 mol•L-1的MgCl2溶液中,含有Cl-个数为NA |
18.在标准状况下CH4、HCl、H2S、NH3均为气体.在标准状况下分别有①13.44L CH4 ②1molHCl分子 ③27.2gH2S ④2.408×1023个NH3分子,下列说法正确的是( )
| A. | 体积:②>③>④>① | B. | 密度:②>③>①>④ | ||
| C. | 质量:②>③>④>① | D. | H原子个数:①>③>④>② |
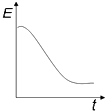
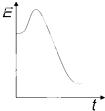
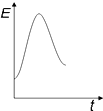
8.下列图示与对应的叙述不相符的是( )


| A. | 图甲表示反应:4CO(g)+2NO2(g)=N2(g)+4CO2(g)△H<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2 | |
| B. | 图乙表示压强对可逆反应2A(g)+2B(g)=3C(g)+D(g)的影响,乙的压强比甲的压强大 | |
| C. | 图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变 | |
| D. | 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)=N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 |
16. 实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
有关数据见下表:
(1)A中加入沸石的作用是防止液体瀑沸.
(2)B中进水口为b(填“a”或“b”)口.
(3)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下.
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?2HBr+H2SO4(浓)=Br2+SO2↑+2H2O(用化学方程式表示).
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是53.3%.
 实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色 液体 | 无色 液体 | 深红棕色 液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(2)B中进水口为b(填“a”或“b”)口.
(3)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下.
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?2HBr+H2SO4(浓)=Br2+SO2↑+2H2O(用化学方程式表示).
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是53.3%.