题目内容
Mg、Al用导线连接后分别浸入到稀硫酸和浓NaOH溶液中构成原电池,试分别写出它们发生的电极反应式。见解析
【试题分析】
稀硫酸为电解质溶液时,Mg、Al都能与之反应,故Mg为负极,铝为正极。故正、负极的电极反应式为:
负极:Mg-2e-=Mg2+
正极:2H++2e-=H2↑
浓NaOH溶液为电解质溶液时,Mg不反应,Al能反应,故Al为负极,Mg为正极。故正、负极的电极反应式为:
负极:2Al+8OH--6e-=2
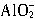 +4H2O
+4H2O正极:6H++6e-=3H2↑

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目