题目内容
【题目】如图是实验室中制备气体或者验证气体性质的装置图 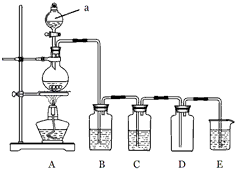
(1)写出用A制取氯气的化学方程式
(2)利用图中装置制备纯净、干燥的氯气,并证明氧化性:Cl2>Fe3+装置B中的溶液的作用为;装置D中加的最佳试剂为(填序号) .
供选试剂:a、浓硫酸 b、FeCl2溶液 c、KSCN与FeCl2的混合溶液 d、无水氯化钙
(3)在如图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具有氧化性和漂白性:B中为少量Na2S溶液、C中为品红溶液,D中应加入足量的(填溶液名称),E中加入溶液(填化学式)
(4)证明碳元素的非金属性比硅元素的强的现象为 , 实验2不严谨之处应如何改进
【答案】
(1)MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)除去氯气中的氯化氢;c
(3)酸性高锰酸钾溶液;Na2SiO3
(4)D中高锰酸钾溶液不褪色,E中溶液变浑浊;将烧杯换成洗气瓶,右端连接盛有碱石灰的干燥
【解析】解:(1)制备氯气是利用装置加热生成,试剂是二氧化锰和浓盐酸加热反应生成,反应的化学方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;所以答案是:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;所以答案是:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;(2)氯气中含有氯化氢气体,通过装置B饱和食盐水可以吸收氯化氢,含亚铁离子的物质被氯气氧化成铁离子使硫氰化钾变红色来来证明Cl2>Fe3+ , 因此选KSCN与FeCl2的混合溶液,
MnCl2+Cl2↑+2H2O;(2)氯气中含有氯化氢气体,通过装置B饱和食盐水可以吸收氯化氢,含亚铁离子的物质被氯气氧化成铁离子使硫氰化钾变红色来来证明Cl2>Fe3+ , 因此选KSCN与FeCl2的混合溶液,
所以答案是:除去氯气中的氯化氢;c;(3)元素的非金属性越强,最高价氧化物对应的水化物酸性越强,利用碳酸的酸性强于硅酸,
二氧化碳能与硅酸钠反应制得硅酸沉淀,由于CO2中混有二氧化硫,二氧化硫也能与硅酸钠溶液反应,
需要酸性高锰酸钾溶液除去,防止干扰检验二氧化碳;
所以答案是:酸性高锰酸钾溶液,Na2SiO3;(4)若D中高锰酸钾溶液不褪色,说明二氧化硫除尽,E中溶液变浑浊,说明含有二氧化碳气体;空气中含有二氧化碳,可能干扰实验,故应排除空气中二氧化碳的干扰,将烧杯换成洗气瓶,右端连接盛有碱石灰的干燥管可排除空气中二氧化碳的干扰,
所以答案是:D中高锰酸钾溶液不褪色,E中溶液变浑浊;将烧杯换成洗气瓶,右端连接盛有碱石灰的干燥.

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择不正确的是( )
选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
A | 己烷(己烯) | 溴水 | 分液 |
B | 淀粉溶液(NaCl) | 水 | 渗析 |
C | CH3CH2OH(CH3COOH) | CaO | 蒸馏 |
D | 肥皂(甘油) | NaCl | 过滤 |
A.A
B.B
C.C
D.D