题目内容
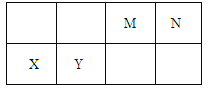
【题目】几种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。下列说法不正确的是
A. 元素的第一电离能X<Y
B. X位于第三周期IIA ,其单质可采用电解熔融其氯代物制备
C. 元素最高价氧化物的水化物中,酸性最强的是HNO3
D. 气体分子(MN)2的电子式为![]()
【答案】A
【解析】试题分析:4种元素都是短周期元素,且为相邻主族,根据元素在周期表中的位置知,M和N位于第二周期、X和Y位于第三周期,X原子核外电子数是M的2倍,Y的氧化物具有两性,则Y是Al元素,根据元素相对位置可知,X是Mg元素、M是C元素、N元素为N元素。A.Mg元素的3s为全充满结构,比较稳定,元素的第一电离能X>Y,故A错误;B.元素X是Mg元素,其原子序数为12,在周期表中的位置是第三周期第IIA族,镁单质可采用电解熔融MgCl2制备,故B正确;C.M、N、X、Y分别是C、N、Mg、Al,元素的非金属性越强,其最高价氧化物的水化物酸性越强,这四种种元素中非金属性最强的是N元素,所以酸性最强的是HNO3,故C正确;D.气体分子(MN)2为(CN)2,其电子式为:![]() ,故D正确;故选A。
,故D正确;故选A。

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案
相关题目