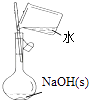题目内容
【题目】在研究金矿床物质组分的过程中,通过分析发现了Cu﹣Ni﹣Zn﹣Sn﹣Fe多金属互化物.
(1)某金属互化物属于晶体,区别晶体和非晶体可通过方法鉴别.该金属互化物原子在三维空间里呈周期性有序排列,即晶体具有性.
(2)基态Ni2+的核外电子排布式;配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4 属于晶体.
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2 . 1mol(SCN)2分子中含有σ键的数目为;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H﹣S﹣C≡N)的沸点低于异硫氰酸(H﹣N=C=S)的沸点,其原因是;
(4)立方NiO(氧化镍)晶体的结构如图﹣1所示,其晶胞边长为apm,列式表示NiO晶体的密度为g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)人工制备的NiO晶体中常存在缺陷(如图﹣2)一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.已知某氧化镍样品组成Ni0.96O,该晶体中Ni3+与Ni2+的离子个数之比为 . 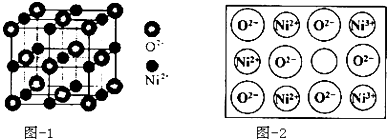
【答案】
(1)X﹣射线衍射实验;自范
(2)1s22s22p63s23p63d8;分子
(3)5NA;异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键
(4)![]() ;1:11
;1:11
【解析】解:(1)晶体和非晶体可通过X﹣射线衍射实验进行鉴别,金属互化物原子在三维空间里呈周期性有序排列,金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于晶体,所以答案是:X﹣射线衍射实验;自范;(2)Ni元素原子核外电子数为28,核外电子排布式为1s22s22p63s23p63d84s2 , 失去4s能级2个电子形成Ni2+ , 故Ni2+离子核外电子排布为:1s22s22p63s23p63d8 , Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于分子晶体,所以答案是:1s22s22p63s23p63d8;分子;(3)(SCN)2的结构式为N≡C﹣S﹣S﹣C≡N,根据[(SCN)2]的结构可知分子中有3个单键和2个碳氮三键,单键为σ键,三键含有1个σ键、2个π键,(SCN)2分子含有5个σ键,故1mol(SCN)2分子中含有σ键的数目为 5NA;由于异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键,所以硫氰酸(H﹣S﹣C≡N)的沸点低于异硫氰酸,所以答案是:5NA;异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键;(4)晶胞中Ni原子数目为1+12× ![]() =4,氧原子数目为8×
=4,氧原子数目为8× ![]() +6×
+6× ![]() =4,晶胞质量为4×
=4,晶胞质量为4× ![]() g,晶胞边长为apm,晶胞体积为(a×10﹣10 cm)3 , NiO晶体的密度为为4×
g,晶胞边长为apm,晶胞体积为(a×10﹣10 cm)3 , NiO晶体的密度为为4× ![]() g÷(a×10﹣10 cm)3=
g÷(a×10﹣10 cm)3= ![]() g/cm3;设1mol Ni0.96O中含Ni3+xmol,Ni2+为(0.96﹣x)mol,根据晶体仍呈电中性,可知 3x+2×(0.96﹣x)=2×1,x=0.08mol Ni2+为(0.96﹣x)mol=0.88mol,即离子数之比为Ni3+:Ni2+=0.08:0.88=1:11,所以答案是:
g/cm3;设1mol Ni0.96O中含Ni3+xmol,Ni2+为(0.96﹣x)mol,根据晶体仍呈电中性,可知 3x+2×(0.96﹣x)=2×1,x=0.08mol Ni2+为(0.96﹣x)mol=0.88mol,即离子数之比为Ni3+:Ni2+=0.08:0.88=1:11,所以答案是: ![]() ;1:11.
;1:11.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
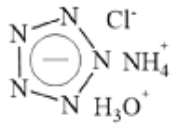
小学生10分钟应用题系列答案【题目】下列有关实验的选项正确的是( )
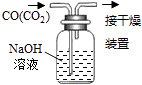
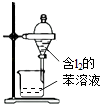
A.配制0.10molL﹣1NaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中I2 , 分出水层后的操作 | D.记录滴定终点读数为12.20mL |
|
|
|
|
A.A
B.B
C.C
D.D