题目内容
A、B、C、D、E都是前20号元素中的常见元素,且核电荷数递增.A原子没有中子;B原子次外层电子数与最外层电子数之差等于电子层数;C元素是地壳中含量最高的元素;4.6g D单质与足量盐酸作用可产生2.24LH2(标准状态下);E的一价阴离子的核外电子排布与Ar的核外电子排布相同.请回答下列问题:
(1)写出A、B、D的元素符号:A
(2)C离子的电子式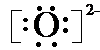
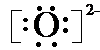 ;E的离子结构示意图
;E的离子结构示意图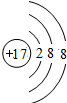
 .
.
(3)实验室里检验E的单质常用的试剂是
(4)写出电解D、E形成化合物的水溶液的化学反应方程式
(5)写出由A、B、C、D形成的化合物与由A、C、E形成的化合物发生反应的化学反应方程式
(1)写出A、B、D的元素符号:A
H
H
;BC
C
;DNa
Na
.(2)C离子的电子式
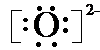
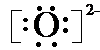


(3)实验室里检验E的单质常用的试剂是
淀粉KI溶液(或试纸)
淀粉KI溶液(或试纸)
.(4)写出电解D、E形成化合物的水溶液的化学反应方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
(5)写出由A、B、C、D形成的化合物与由A、C、E形成的化合物发生反应的化学反应方程式
HClO4+NaHCO3=NaClO4+H2O+CO2↑
HClO4+NaHCO3=NaClO4+H2O+CO2↑
.分析:A、B、C、D、E都是前20号元素中的常见元素,且核电荷数递增.A原子没有中子,则A为H元素;C元素是地壳中含量最高的元素,则C为O元素;B原子次外层电子数与最外层电子数之差等于电子层数,原子序数小于氧元素,B有2个电子层,最外层电子数为4,故B为C元素;4.6g D单质与足量盐酸作用可产生2.24LH2(标准状态下),D为金属,令D的摩尔质量为xg/mol,化合价为y,则
×y=
×2,即23y=x,为前20号元素中的常见元素,故y=1,x=23,则D为Na元素;E的一价阴离子的核外电子排布与Ar的核外电子排布相同,则E为Cl元素.
| 4.6g |
| xg/mol |
| 2.24L |
| 22.4L/mol |
解答:解:A、B、C、D、E都是前20号元素中的常见元素,且核电荷数递增.A原子没有中子,则A为H元素;C元素是地壳中含量最高的元素,则C为O元素;B原子次外层电子数与最外层电子数之差等于电子层数,原子序数小于氧元素,B有2个电子层,最外层电子数为4,故B为C元素;4.6g D单质与足量盐酸作用可产生2.24LH2(标准状态下),D为金属,令D的摩尔质量为xg/mol,化合价为y,则
×y=
×2,即23y=x,为前20号元素中的常见元素,故y=1,x=23,则D为Na元素;E的一价阴离子的核外电子排布与Ar的核外电子排布相同,则E为Cl元素.
(1)由上述分析可知,A 为H;B 为C;D为Na.
故答案为:H; C; Na;
(2)C为O元素,氧原子获得2个电子形成氧离子,电子式为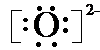 .E为Cl元素,氯离子质子数为
.E为Cl元素,氯离子质子数为
17,核外电子数为18,有3个电子层,最外层电子数为8,氯离子结构示意图为 .
.
故答案为: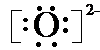 ;
; ;
;
(3)氯气有强氧化性,可以使淀粉KI溶液(或试纸)变蓝,故实验室里检验氯气常用淀粉KI溶液(或试纸)
故答案为:淀粉KI溶液(或试纸).
(4)电解氯化钠溶液,生成氢氧化钠、氯气、氢气,电解反应方程式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑.
故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;
(5)由A、B、C、D形成的化合物为NaHCO3,由A、C、E形成的化合物为HClO4,二者发生反应生成高氯酸钠、水、二氧化碳,反应方程式为:HClO4+NaHCO3=NaClO4+H2O+CO2↑.
故答案为:HClO4+NaHCO3=NaClO4+H2O+CO2↑.
| 4.6g |
| xg/mol |
| 2.24L |
| 22.4L/mol |
(1)由上述分析可知,A 为H;B 为C;D为Na.
故答案为:H; C; Na;
(2)C为O元素,氧原子获得2个电子形成氧离子,电子式为
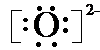 .E为Cl元素,氯离子质子数为
.E为Cl元素,氯离子质子数为17,核外电子数为18,有3个电子层,最外层电子数为8,氯离子结构示意图为
 .
.故答案为:
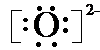 ;
; ;
;(3)氯气有强氧化性,可以使淀粉KI溶液(或试纸)变蓝,故实验室里检验氯气常用淀粉KI溶液(或试纸)
故答案为:淀粉KI溶液(或试纸).
(4)电解氯化钠溶液,生成氢氧化钠、氯气、氢气,电解反应方程式为2NaCl+2H2O
| ||
故答案为:2NaCl+2H2O
| ||
(5)由A、B、C、D形成的化合物为NaHCO3,由A、C、E形成的化合物为HClO4,二者发生反应生成高氯酸钠、水、二氧化碳,反应方程式为:HClO4+NaHCO3=NaClO4+H2O+CO2↑.
故答案为:HClO4+NaHCO3=NaClO4+H2O+CO2↑.
点评:考查元素推断、常用化学用语、元素及化合物的性质等,难度不大,推断元素是解题的关键.

练习册系列答案
相关题目
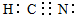
 CH3COOH+OH-
CH3COOH+OH- 已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示) 示)位于该正方体的顶点和面心,该化合物的化学式是
示)位于该正方体的顶点和面心,该化合物的化学式是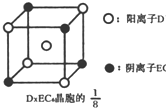
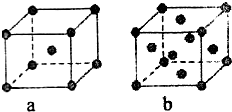 已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.
已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.