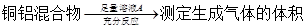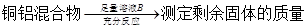题目内容
某化学小组在常温下测定一定质量的某铁铝混合物中铁的质量分数,设计了如下实验方案:
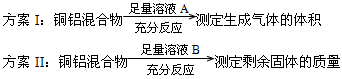
方案Ⅰ:铁铝混合物
测定生成气体的体积
方案Ⅱ:铁铝化合物
测定剩余固体的质量
下列有关叙述中不正确的是( )
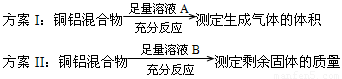
方案Ⅰ:铁铝混合物
| 足量溶液A |
| 充分反应 |
方案Ⅱ:铁铝化合物
| 足量溶液B |
| 充分反应 |
下列有关叙述中不正确的是( )
| A、溶液A和B都可以用NaOH溶液 |
| B、溶液A和B都可以用稀盐酸 |
| C、方案Ⅰ比方案Ⅱ易产生误差 |
| D、在实验室方案Ⅱ比方案Ⅰ易实施 |
分析:在知道混合物质量的前提下,方案I可以使用碱液,此时气体是由铝生成的,由此可求出铝的量;也可以使用酸液,此时气体是由铁铝共同生成,根据混合物的质量、生成气体的体积分别列一个方程,联立即可解除铁铝的量;但方案II中由于是根据剩余固体的质量来解题,所以只能用碱液;再结合具体的实验操作来解本题.
解答:解:A、在方案I中,能与NaOH溶液反应的只有铝,根据生成的氢气可以计算出混合物中铝的质量,从而能计算出铁的质量及铁在混合物中的质量分数,故溶液A可为NaOH溶液;在方案II中,铁与NaOH溶液不反应,铝与NaOH溶液反应,剩余的固体为铁,可以计算出铁的质量分数,故A正确.
B、铁和铝都均可以与稀盐酸反应,利用测量气体的体积,可以计算出混合物中铁、铝的质量,故方案I可以用稀盐酸;由于稀盐酸足量,方案II中不会有固体剩余,所以方案II不能用稀盐酸,故B错误.
C、反应是在常温下进行的,所得气体的体积是常温下的体积,必须换算成标况下的体积才能计算;收集气体时容易由于装置气密性不好、排气法收集时会随着空气排出去一部分、反应装置中有气体残留等问题导致产生较大的误差,故C正确.
D、测量气体的体积不如测量固体的质量简单易操作,故D正确.
故选:B.
B、铁和铝都均可以与稀盐酸反应,利用测量气体的体积,可以计算出混合物中铁、铝的质量,故方案I可以用稀盐酸;由于稀盐酸足量,方案II中不会有固体剩余,所以方案II不能用稀盐酸,故B错误.
C、反应是在常温下进行的,所得气体的体积是常温下的体积,必须换算成标况下的体积才能计算;收集气体时容易由于装置气密性不好、排气法收集时会随着空气排出去一部分、反应装置中有气体残留等问题导致产生较大的误差,故C正确.
D、测量气体的体积不如测量固体的质量简单易操作,故D正确.
故选:B.
点评:本题以铝、铁的性质为依托,考查了实验方案的设计与评价,有综合性但难度不大.

练习册系列答案
相关题目
某化学小组在常温下测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ: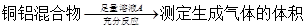
方案Ⅱ: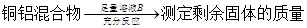
下列有关判断中不正确的是
| A.溶液A和B均可以是盐酸或NaOH溶液 |
| B.溶液A和B均可以选用稀硝酸 |
| C.若溶液B选用浓硝酸,则测得铜的质量分数偏小 |
| D.实验室方案II更便于实施 |