题目内容
(8分)某温度下,在2L密闭容器中,3种气态物质 X、Y、Z的物质的量随时间变化曲线如图,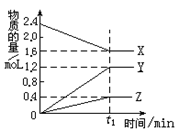
⑴① 该反应的化学方程式是_____________________。
②在t1min时,该反应达到了__________状态,下列可作为判断反应已达到该状态的是__________
| A.X、Y、Z的反应速率相等 | B.X、Y的反应速率比为2:3 |
| C.容器内气体压强保持不变 | D.生成1molZ的同时生成2molX |
②两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是______同学。
(8分)⑴① 2X  3Y + Z 。② 平衡, CD 。
3Y + Z 。② 平衡, CD 。
⑵ ① 2NH3(g)  N2(g) + 3H2(g) △H=+92KJ/mol。② 乙
N2(g) + 3H2(g) △H=+92KJ/mol。② 乙
解析

练习册系列答案
相关题目

 某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质
某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质 3Y+Z
3Y+Z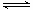 B(g) + C(g);ΔH = −48.25 kJ/L
B(g) + C(g);ΔH = −48.25 kJ/L