题目内容
 某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质
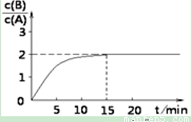
某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.依图回答:
(1)该反应的化学方程式可表示为
2X 3Y+Z
3Y+Z
 3Y+Z
3Y+Z2X 3Y+Z
3Y+Z
. 3Y+Z
3Y+Z(2)反应起始至t1min(设t1=5),Y的平均反应速率是
0.12mol?L-1?min-1
0.12mol?L-1?min-1
.(3)在t1min时,该反应达到了
化学平衡
化学平衡
状态,下列可判断反应已达到该状态的是D、F
D、F
(选填字母)A.X、Y、Z的反应速率相等 B.X、Y的反应速率比为2:3
C.混合气体的密度不变 D.生成1molZ的同时生成2molX
E.X、Y、Z物质的量之比等于系数比 F.混合气体的总压强不再发生改变.
分析:(1)化学反应中,各物质的物质的量的变化值与化学计量数呈正比,以此书写化学方程式;
(2)根据v=
计算反应速率;
(3)当反应中各物质的物质的量不变变化时,反应达到平衡状态,各物质的浓度不变,由此衍生的一些物理量不变.
(2)根据v=
| △c |
| △t |
(3)当反应中各物质的物质的量不变变化时,反应达到平衡状态,各物质的浓度不变,由此衍生的一些物理量不变.
解答:解:(1)由图象可以看出,X的物质的量逐渐减小,则X为反应物,Y、Z的物质的量逐渐增多,作为Y、Z为生成物,当反应到达2min时,△n(X)=0.8mol,△n(Y)=1.2mol,△n(Z)=0.4mol,化学反应中,各物质的物质的量的变化值与化学计量数呈正比,
则△n(X):△n(Y):△n(Z)=2:3:1,所以反应的化学方程式为:2X 3Y+Z;
3Y+Z;
故答案为:2X 3Y+Z;
3Y+Z;
(2)v(Y)=
=
=0.12mol?L-1?min-1,
故答案为:0.12mol?L-1?min-1;
(3)在t1min时,反应中各物质的物质的量不变变化时,反应达到平衡状态,
A.由于各物质的化学计量数不等,则X、Y、Z的反应速率相等不能说明是否达到平衡状态,故A错误;
B.化学反应速率之比等于化学计量数之比,无论是否达到平衡状态,X、Y的反应速率比都为2:3,故B错误;
C.由于反应在体积不变的密闭容器中进行,反应过程中气体的体积不变,质量不变,则混合气体的密度不变,不能判断是否达到平衡状态,故C错误;
D.生成1molZ的同时生成2molX,说明正逆反应速率相等,达到平衡状态,故D正确;
E.无论是否达到平衡状态,X、Y、Z物质的量之比都等于系数比,不能说明达到平衡状态,故E错误;
F.反应达到平衡状态时,各物质的物质的量不变,则混合气体的总压强不再发生改变,故F正确.
故D、F正确,
故答案为:化学平衡; D、F.
则△n(X):△n(Y):△n(Z)=2:3:1,所以反应的化学方程式为:2X
 3Y+Z;
3Y+Z;故答案为:2X
 3Y+Z;
3Y+Z;(2)v(Y)=
| △c |
| △t |
| ||
| 5min |
故答案为:0.12mol?L-1?min-1;
(3)在t1min时,反应中各物质的物质的量不变变化时,反应达到平衡状态,
A.由于各物质的化学计量数不等,则X、Y、Z的反应速率相等不能说明是否达到平衡状态,故A错误;
B.化学反应速率之比等于化学计量数之比,无论是否达到平衡状态,X、Y的反应速率比都为2:3,故B错误;
C.由于反应在体积不变的密闭容器中进行,反应过程中气体的体积不变,质量不变,则混合气体的密度不变,不能判断是否达到平衡状态,故C错误;
D.生成1molZ的同时生成2molX,说明正逆反应速率相等,达到平衡状态,故D正确;
E.无论是否达到平衡状态,X、Y、Z物质的量之比都等于系数比,不能说明达到平衡状态,故E错误;
F.反应达到平衡状态时,各物质的物质的量不变,则混合气体的总压强不再发生改变,故F正确.
故D、F正确,
故答案为:化学平衡; D、F.
点评:本题考查化学平衡的图象问题以及平衡状态的判断,题目难度中等,注意把握图象的分析和平衡状态的判断,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(8分)某温度下,在2L密闭容器中,3种气态物质 X、Y、Z的物质的量随时间变化曲线如图,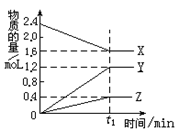
⑴① 该反应的化学方程式是_____________________。
②在t1min时,该反应达到了__________状态,下列可作为判断反应已达到该状态的是__________
| A.X、Y、Z的反应速率相等 | B.X、Y的反应速率比为2:3 |
| C.容器内气体压强保持不变 | D.生成1molZ的同时生成2molX |
②两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是______同学。

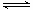 B(g) + C(g);ΔH = −48.25 kJ/L
B(g) + C(g);ΔH = −48.25 kJ/L