题目内容
【题目】100mL某混合液中,硝酸和硫酸的物质量浓度分别是0.4mol·L-1,0.1mol·L-1,向该混合液中加入1.92g铜粉,加热,待充分反应后,所得溶液中铜离子物质量浓度是( )
A.0.15 mol·L-1B.0.225 mol·L-1C.0.35 mol·L-1D.0.45 mol·L
【答案】B
【解析】
溶液中n(H+)=0.1mol/L×2×0.1L+0.4mol/L× 0.1L=0.06mol,n(Cu)=![]() ,反应计算如下:
,反应计算如下:
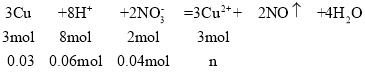
![]()
由上式的物质的量关系可知Cu过量和NO3-过量,因此用H+进行计算,
n=0.0225mol,n(Cu2+)=![]() ×0.06mol=0.0225mol,c(Cu2+)=
×0.06mol=0.0225mol,c(Cu2+)=![]() =
=![]() ,正确答案B。
,正确答案B。

练习册系列答案
相关题目
【题目】有两份溶液,其中所含溶质相同,设其摩尔质量为M g/mol。根据下表信息,回答有关问题:
项目 | 溶质的质量分数 | 溶液的密度/(g·cm-3) |
第一份溶液 | ω1 | ρ1 |
第二份溶液 | ω2 | ρ2 |
(1)第一份溶液中,溶质的物质的量浓度为_______。
(2)取等质量两份溶液混合,则所得混合液中溶质的质量分数ω3=_____。
(3)若有ω1>ω2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为ω4,试比较ω3、ω4的相对大小____;___。