题目内容
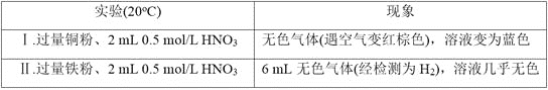
【题目】铜及其化合物具有广泛的应用。回答下列问题:
(1)CuSO4中阳离子的基态核外电子排布式为________。
(2)S、O、N三种元素的第一电离能由小到大的顺序为_________(填元素符号)。
(3)Cu(NO3)2溶液中通入足量NH3能生成配合物[Cu(NH3)4](NO3)2,其中NH3的空间构型为____。
(4)[Cu(NH3)4](NO3)2属于_____晶体。
(5)CuSO4溶液中加入过量KCN能生成配离子[Cu(CN)4]2-,1 mol CN-中含有的π键数目为____。
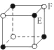
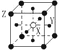
(6)已知Cu2O晶胞结构如图所示,该晶胞原子坐标参数A为(0,0,0),B为(1,0,0),C为(![]() ,
,![]() ,
,![]() )。则D原子的坐标参数代表_____原子(填元素符号)。
)。则D原子的坐标参数代表_____原子(填元素符号)。
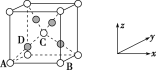
(7)金属铜的晶体晶胞中Cu原子的空间利用率是____。
【答案】1s22s22p63s23p63d9(或[Ar]3d9) S<O<N 三角锥形 离子 2NA Cu 74%
【解析】
(1)CuSO4中阳离子为Cu2+,其价电子排布式为:1s22s22p63s23p63d9(或[Ar]3d9),故答案为:1s22s22p63s23p63d9(或[Ar]3d9);
(2)同周期主族元素的第一电离能,随着原子序数的增大,有增大的趋势,但第ⅤA族大于第ⅥA族元素,同主族元素,随着原子序数的增加,第一电离能逐渐减小,则S、O、N三种元素的第一电离能由大到小的顺序为:N>O>S,故答案为:N>O>S;
(3)根据价层电子对互斥理论确定微粒空间构型,价层电子对个数=σ键+孤电子对个数,孤电子对个数=![]() (a-xb),a为中心原子的价电子数,x为与中心原子结合的原子个数,b为与中心原子结合的原子最多能接受的电子数, NH3中价层电子对个数=3+1=4,是三角锥形型,故答案为:三角锥形;
(a-xb),a为中心原子的价电子数,x为与中心原子结合的原子个数,b为与中心原子结合的原子最多能接受的电子数, NH3中价层电子对个数=3+1=4,是三角锥形型,故答案为:三角锥形;
(4)[Cu(NH3)4](NO3)2是[Cu(NH3)4]2+与NO3-形成的离子化合物,属于离子晶体,故答案为:离子晶体;
(5)CN与N2互为等电子体,CN中C、N之间形成C≡N三键,三键含有1个σ键、2个π键,1molCN中含有的2molπ键,1molCN中含有的π键数目为:2NA,故答案为:2NA;
(6)晶胞原子坐标参数A为(0,0,0)、B为(1,0,0)、C为(![]() ,
,![]() ,
,![]() ),如图坐标系中,A为处于坐标系中的原点(定义为O),则C处于晶胞体心位置,A、D、C的连线处于体对角线线上,且D处于A、C连线的中点位置,故D到晶胞左侧面距离为
),如图坐标系中,A为处于坐标系中的原点(定义为O),则C处于晶胞体心位置,A、D、C的连线处于体对角线线上,且D处于A、C连线的中点位置,故D到晶胞左侧面距离为![]() 、到晶胞前面的距离为
、到晶胞前面的距离为![]() ,到晶胞下底面距离为
,到晶胞下底面距离为![]() ,则D的参数为(
,则D的参数为(![]() ,
,![]() ),晶胞中白色球数目为:1+8×
),晶胞中白色球数目为:1+8×![]() =2,黑色球数目为:4,二者数目之比为1:2,而化学式为Cu2O,故黑色球为Cu原子、白色球为O原子,即D表示Cu原子,故答案为:Cu;
=2,黑色球数目为:4,二者数目之比为1:2,而化学式为Cu2O,故黑色球为Cu原子、白色球为O原子,即D表示Cu原子,故答案为:Cu;
(7)金属铜是面心立方最密堆积方式,Cu原子处于顶点与面心,顶点Cu原子与面心Cu原子相邻,每个顶点为8个晶胞共用,每个面为2个晶胞共用,设Cu原子半径为r,则面对角线是4r,晶胞棱长为2![]() r,晶胞体积为(2
r,晶胞体积为(2![]() r)3,晶胞中Cu原子数目为8×
r)3,晶胞中Cu原子数目为8×![]() +6×
+6×![]() =4,晶胞中Cu原子总体积为4×
=4,晶胞中Cu原子总体积为4×![]() πr3,该晶胞中Cu原子的空间利用率为
πr3,该晶胞中Cu原子的空间利用率为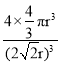 ×100%=74%,故答案为:74%。
×100%=74%,故答案为:74%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
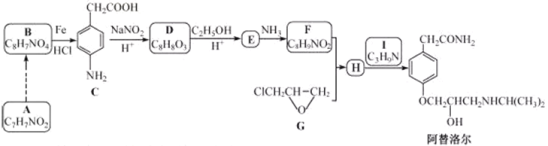
小学生10分钟应用题系列答案【题目】制备钙掺杂纳米Fe3O4,并模拟吸附废水中磷元素的主要实验流程如下:

已知:①CaO2能氧化溶液中的FeCl2,反应生成Fe(OH)3和Fe3+。
②掺杂的Ca2+嵌入Fe3O4中,洗涤时不损失,吸附时不形成Ca3(PO4)2等沉淀。
③溶液的pH对吸附剂表面所带电荷有影响。pH越高,表面所带负电荷越多; pH越低,表面所带正电荷越多。
(1)向FeCl2、FeCl3混合溶液中滴加NaOH溶液,一定条件下反应生成Fe3O4,其离子方程式为___________。
(2)步骤Ⅱ调节pH至11,共沉淀需在70℃条件下进行,适宜的加热方式为________。为提高共沉淀效果,还可采取的措施为_______________。
(3)磷元素的吸附效果、H3PO4水溶液中含磷物种分布分数与pH的关系分别如图1和图2所示。

①步骤Ⅳ用KH2PO4溶液模拟废水,测得酸性条件下(pH > 2)对磷元素吸附量较大,原因是:pH越低,吸附剂表面所带正电荷越多,有利于吸附阴离子;___________________
②步骤Ⅴ将吸附剂取出,用碱液解吸回收磷。结合表中数据,分析钙掺杂纳米Fe3O4吸附剂与其他类型吸附剂相比的优势有:________。
不同类型吸附剂对磷酸盐吸附能力比较
吸附剂 | 本产品 | 纯Fe3O4 | 陶瓷材质 |
吸附量/mg·g-1 | 24.1 | 5.0 | 12.5 |
(4)请设计从步骤Ⅱ反应结束后的烧瓶中获取钙掺杂纳米Fe3O4产品的实验方案:用磁铁将沉淀物和溶液分离,______________,用筛网筛分得到产品 (实验中须使用的试剂和仪器有:蒸馏水、无水乙醇、pH计、研钵、烘箱)。