题目内容
运用元素周期律分析下面的推断,其中错误的是( )
①113号元素的单质是一种金属,它的氧化物的水化物不能与强碱反应;
②砹(At2)是一种有色固体,HAt很不稳定,AgAt是有色难溶于水的固体;
③硫酸锶是难溶于水和盐酸的有色固体;
④H2S比水的还原性弱,但H2S比水的稳定性强;
⑤周期表中钠在钾的上方,因此非金属性钠比钾弱,单质的熔点钠也比钾低;
⑥第二周期非金属元素(除稀有气体元素)原子半径小,得电子能力强,其气态氢化物的水溶液均呈酸性.
①113号元素的单质是一种金属,它的氧化物的水化物不能与强碱反应;
②砹(At2)是一种有色固体,HAt很不稳定,AgAt是有色难溶于水的固体;
③硫酸锶是难溶于水和盐酸的有色固体;
④H2S比水的还原性弱,但H2S比水的稳定性强;
⑤周期表中钠在钾的上方,因此非金属性钠比钾弱,单质的熔点钠也比钾低;
⑥第二周期非金属元素(除稀有气体元素)原子半径小,得电子能力强,其气态氢化物的水溶液均呈酸性.
| A、③④⑤⑥ | B、④⑤⑥ |
| C、②③④ | D、③④⑥ |
考点:同一主族内元素性质递变规律与原子结构的关系,非金属在元素周期表中的位置及其性质递变的规律,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:同主族,从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,对应的氢化物的稳定性逐渐减弱,原子半径逐渐增大,同主族元素的性质具有相似性和递变性,以此解答该题.
解答:
解:①113号元素位于第ⅢA族,金属性比Al强,它的氧化物的水化物不能与强碱反应,故①正确;
②砹(At)属于卤素单质,从上到下氢化物稳定性逐渐减弱,单质由气体过渡为固体,所以At为有色固体,HAt不稳定,故②正确;
③硫酸锶(SrSO4)是难溶于水的白色固体,故③错误;
④非金属性O>S,H2S比水的还原性强,稳定性比水的弱,故④错误;
⑤钠和钾都具有较强的金属性,不具有非金属性,单质的熔点钠比钾高,故⑤错误;
⑥氨气水溶液呈碱性,故⑥错误.
故选A.
②砹(At)属于卤素单质,从上到下氢化物稳定性逐渐减弱,单质由气体过渡为固体,所以At为有色固体,HAt不稳定,故②正确;
③硫酸锶(SrSO4)是难溶于水的白色固体,故③错误;
④非金属性O>S,H2S比水的还原性强,稳定性比水的弱,故④错误;
⑤钠和钾都具有较强的金属性,不具有非金属性,单质的熔点钠比钾高,故⑤错误;
⑥氨气水溶液呈碱性,故⑥错误.
故选A.
点评:本题考查同主族元素的性质的相似性和递变性,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握元素周期律的递变性和相似性.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
下列分子式或结构式一定表示葡萄糖的是( )
| A、C6H12O6 |
| B、CH2OH(CHOH)4CHO |
| C、CH2OH(CHOH)3CHO |
D、 |
甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )
| A、CH3Cl只有一种空间结构(不存在同分异构体) |
| B、CH4是非极性分子 |
| C、CH2Cl2只有一种空间结构 |
| D、CH4中的四个键的键角和键长都相等 |
根据电子排布的特点,原子序数为30的元素X在周期表中属于( )
| A、s区 | B、p区 |
| C、d 区 | D、ds区 |
苯环上有一个-C4H9和一个-C3H7两个取代基的有机物共有同分异构体( )
| A、12种 | B、4种 |
| C、8种 | D、24种 |
(双选)下列物质在浓H2SO4作用下能发生消去反应的是( )
| A、CH3OH |
| B、(CH3)3COH |
| C、(CH3)3CCH2OH |
D、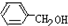 |
E、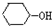 |
下列说法正确的是( )
| A、原子的L层上的电子数为奇数的元素一定是主族元素 |
| B、同一周期的ⅡA族和ⅢA族元素的原子序数之差一定为1 |
| C、相邻两个周期的同一主族元素的原子序数之差等于上一周期所含元素种类 |
| D、主族序数等于周期序数的元素一定为金属元素 |
1.28g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到448mL气体(标况).将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积是( )
| A、168mL |
| B、224mL |
| C、336mL |
| D、504mL |
将一小块钠放入CuSO4溶液中,观察到现象是( )
| A、钠溶解,有Cu析出,并有气体产生 |
| B、钠溶解,有蓝色沉淀,有氢气产生 |
| C、有气体产生,无沉淀产生 |
| D、钠在液面逐渐消失,有气体产生和蓝色沉淀 |