题目内容
【题目】氮化铝(AIN)是一种新型无机非金属材料。某AlN样品仅含有趾Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。
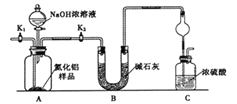
(1)上图C装置中球形干燥管的作用是_____________________。
(2)实验步骤:组装好实验装置,检查好装置气密性再加入实验药品,接下来关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化,通入氮气的目的____________________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见__________________。
【方案2】用如图装置测定mg样品中A1N的纯度(部分夹持装置已略去)。
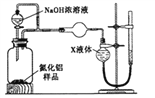
(4)为测定生成气体的体积,量气装置中的X液体不可以是_____________________。
A.NH4Cl溶液 b.CCl4 c.H2O d.苯
(5)若ag样品完全反应,测得生成气体的体积为bmL(已转换为标准状况),则AlN的质量分数是__________。
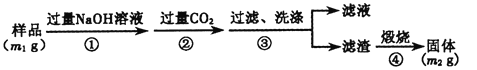
(6)写出步骤中发生的化学反应方程式_______________________________。
(7)若在步骤③中未洗涤,测定结果将______(填“偏高”、“偏低”或“无影响”)。
【答案】 防倒吸 把装置中残留的氨气全部赶入C装置 C装置出处连接一个干燥装置 a,c (416/224a)% AlN+NaOH+H2O=NaAlO2+NH3↑ 偏高
【解析】(1)分析装置和仪器作用分析,氨气是与浓硫酸能发生反应的气体,易发生倒吸,图C装置中球形干燥管的作用是防止倒吸的作用;
(2)组装好实验装置,原理可知气体制备需要先检查装置气密性,加入实验药品。接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是将反应生成的氨气全部转移到装置C中被浓硫酸吸收,准确测定装置C的增重计算;
(3)装置存在缺陷是空气中的水蒸气和二氧化碳也可以进入装置C,使测定结果偏高,需要连接一个盛碱石灰干燥管;
(4)依据氨气极易溶于水的性质分析,a.氨气极易溶于水,不能用排NH4Cl溶液的方法测定气体体积,故a错误;b. CCl4不能溶解氨气,可以用排四氯化碳溶液的方法测定氨气体积,故b正确;c.氨气极易溶于水,不能排水法测定,故c错误;d.氨气不溶于苯,可以利用排出苯溶液,测定氨气的体积,故d正确;则测量气体装置中的X液体不可以是a、c。
(5)氮化铝(AIN)与氢氧化钠溶液反应方程式:AIN+NaOH+H2O═NaAIO2+NH3↑,则n(NH3)=n(AIN)=bmL×10-3/22.4L/mol,则AlN的质量分数= [(bmL×10-3/22.4L/mol)×41g/mol/ag] ×100%=(41b/224a)%。
(6)氮化铝(AIN)与氢氧化钠溶液反应方程式:AlN+NaOH+H2O═NaAlO2+NH3↑;
(7)若在步骤③中未洗涤,沉淀不洗涤得到滤渣质量会增大,测定结果会偏高。

 一本好题口算题卡系列答案
一本好题口算题卡系列答案