题目内容
周期表前20号元素中,某两种元素的原子序数相差3,周期数相差1,它们形成化合物时原子数之比为1∶2。写出这些化合物的化学式____________。
解析:由于两种元素相差一个周期且原子序数相差3,则必为ⅠA族元素与上周期的ⅥA族元素,或ⅡA族的元素与上一周期的ⅦA族的元素。若它们为二、三周期的元素,则非金属可为O、F,金属为Na、Mg;若为三、四周期的元素则金属为K、Ca,非金属应为Cl、S,所以可形成的原子个数比为1∶2的化合物为:Na2O、K2S、MgF2、CaCl2。
答案:Na2O、K2S、MgF2、CaCl2

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
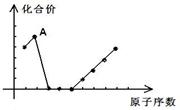
图中曲线表示元素周期表前20号元素中的某些元素的原子序数(按递增顺序连续排列)及其常见最高化合价的关系,其中A点表示的元素是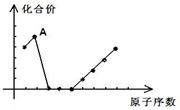
| A.Si | B.Al |
| C.O | D.N |
 图中曲线表示元素周期表前20号元素中的某些元素的原子序数(按递增顺序连续排列)及其常见最高化合价的关系,其中A点表示的元素是( )
图中曲线表示元素周期表前20号元素中的某些元素的原子序数(按递增顺序连续排列)及其常见最高化合价的关系,其中A点表示的元素是( )