题目内容
氯气在生产生活中应用广泛。实验室可用MnO2与浓盐酸反应制取,反应原理如下:MnO2+4HCl(浓)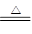 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)若制得标准状况下11.2 L Cl2,则被氧化的HCl为___________mol。
(2)多余的氯气可用NaOH溶液吸收,反应的离子方程式为__________。
(3)海底蕴藏着丰富的锰结核矿,其主要成分是MnO2。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如下图所示:

①步骤Ⅰ中, 试剂甲必须具有的性质是____________(填序号)。
A.氧化性B.还原性C.酸性
②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050 mol MnO2时,消耗0.10 mol·L-1的NaClO3溶液200 mL,该反应的离子方程式为___________________________。
(4)用100mL12.0 mol·L-1的浓盐酸与足量MnO2混合后,加热,反应产生的氯气物质的量远远少于0.30 mol,请你分析可能的原因为___________________________。
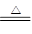 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)若制得标准状况下11.2 L Cl2,则被氧化的HCl为___________mol。
(2)多余的氯气可用NaOH溶液吸收,反应的离子方程式为__________。
(3)海底蕴藏着丰富的锰结核矿,其主要成分是MnO2。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如下图所示:

①步骤Ⅰ中, 试剂甲必须具有的性质是____________(填序号)。
A.氧化性B.还原性C.酸性
②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050 mol MnO2时,消耗0.10 mol·L-1的NaClO3溶液200 mL,该反应的离子方程式为___________________________。
(4)用100mL12.0 mol·L-1的浓盐酸与足量MnO2混合后,加热,反应产生的氯气物质的量远远少于0.30 mol,请你分析可能的原因为___________________________。
(每空2分,共10分)
(1)1
(2)Cl2+2OH?=Cl?+ClO?+H2O
(3)① b ②2ClO3?+5Mn2++4H2O=5MnO2↓+Cl2↑+8H+
(4)随着反应的进行,盐酸浓度减小,反应终止。
(1)1
(2)Cl2+2OH?=Cl?+ClO?+H2O
(3)① b ②2ClO3?+5Mn2++4H2O=5MnO2↓+Cl2↑+8H+
(4)随着反应的进行,盐酸浓度减小,反应终止。
试题分析:(1)根据化学方程式可知被氧化的HCl与Cl2的对应关系为:2HCl~Cl2,则被氧化的HCl=2n(Cl2 )=2×11.2L÷22.4L/mol=1mol。
(2)Cl2与NaOH反应生成NaCl、NaClO、H2O,进而可写成离子方程式。
(3)①步骤I中,Mn元素的化合价由+4价降低为+2价,则试剂甲应具有还原性,故答案为:b;②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050mol MnO2时,消耗0.10mol?L-1 的NaClO3溶液200mL,设还原产物中Cl的化合价为x,则由电子守恒可知,0.05mol×(4-2)=0.1mol/L×0.2L×(5-x),解得x=0,即生成氯气,则离子反应为2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+。
(4)因为MnO2与浓盐酸加热才能生成Cl2,随着反应的进行,盐酸浓度减小,变为稀盐酸后反应终止。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目



 □CO2+□K2SO4+□MnSO4+□H2O
□CO2+□K2SO4+□MnSO4+□H2O
 2NaHSO4+MnSO4+2H2O+I2
2NaHSO4+MnSO4+2H2O+I2 xOH-+ N2+4H2O。下列有关说法正确的是
xOH-+ N2+4H2O。下列有关说法正确的是