题目内容
6. 肼和氧气在相同催化剂和不同温度下生成的产物如图所示.已知在800℃下,容积固定的密闭容器中发生反应①、②:
肼和氧气在相同催化剂和不同温度下生成的产物如图所示.已知在800℃下,容积固定的密闭容器中发生反应①、②:N2H4(g)+O2(g)$\stackrel{催化剂}{→}$N2(g)+2H2O(g) ①
N2H4(g)+2O2(g)$\stackrel{催化剂}{→}$2NO(g)+2H2O(g) ②
下列描述可说明两反应均达到平衡的是( )
| A. | v(N2)=v(NO) | |
| B. | 反应①的△H保持恒定 | |
| C. | 体系的密度不再发生变化 | |
| D. | 混合气体的平均相对分子质量不再发生变化 |
分析 反应到达平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断.
解答 解:A.v(N2)=v(N2H4),未体现正逆反应的关系,故A错误;
B.只要化学方程式不变,其△H保持恒定,与平衡状态无关,故B错误;
C.容器体积不变,反应前后都是气体,气体质量始终不变,说明密度始终不变,密度不变不能说明反应达到平衡状态,故C错误;
D.混合气体的平均相对分子质量不再发生变化,说明气体物质的量不变,已达平衡,故D正确;
故选D;
点评 本题考查了化学平衡状态的判断,注意化学平衡状态的标志正逆反应速率相等和各组分浓度不变,题目难度不大.

练习册系列答案
相关题目
2.电负性差值为零时,可形成( )
| A. | 极性共价键 | B. | 非极性共价键 | C. | 金属键 | D. | 离子键 |
1.常温常压下,向2L密闭容器中加入一定量的A和B气体,发生反应2A(g)+2B(g)?2Q(g)+W(g),△H=M kJ•mol-1,3min后,反应达到平衡,相关数据如下表:则下列说法正确的是( )
| 反应时间/min | n(A)/mol | n(B)/mol |
| 0 | 4 | 4 |
| 0.5 | 3.2 | |
| 2 | 2.4 | |
| 3 | 1.0 |
| A. | 反应在前0.5min时,n(W)=0.6mol | |
| B. | 2min时,反应的平均反应速率为V(Q)=0.48mol/L•s | |
| C. | 相同温度条件下,向平衡后的容器中再充入2mol Q和2mol W时,v(正)>v(逆) | |
| D. | 相同温度下,平衡时的平衡常数为27L•mol-1 |
11. 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率.
(1)除如图装置所示的实验用品外,还需要的一件实验用品是秒表.
(2)圆底烧瓶中反应现象:溶液变浑浊,并有刺激性气体产生,写出所发生反应的离子方程式为S2O32-+2H+═H2O+S↓+SO2↑.
(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水.
(4)利用该化学反应,试简述测定反应速率的其他方法:测定一段时间内生成硫沉淀的质量(或实时测定溶液中氢离子浓度)(写一种).Ⅱ.探究化学反应速率的影响因素为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表.(已知 I2+2S2O${\;}_{3}^{2-}$═S4O${\;}_{6}^{2-}$+2I-,其中Na2S2O3溶液均足量)
(5)表中Vx=4mL,T1、T2、T3的大小关系是T1<T2<T3.
 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率.
(1)除如图装置所示的实验用品外,还需要的一件实验用品是秒表.
(2)圆底烧瓶中反应现象:溶液变浑浊,并有刺激性气体产生,写出所发生反应的离子方程式为S2O32-+2H+═H2O+S↓+SO2↑.
(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水.
(4)利用该化学反应,试简述测定反应速率的其他方法:测定一段时间内生成硫沉淀的质量(或实时测定溶液中氢离子浓度)(写一种).Ⅱ.探究化学反应速率的影响因素为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表.(已知 I2+2S2O${\;}_{3}^{2-}$═S4O${\;}_{6}^{2-}$+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | T1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | T2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | T3 |
15.下列说法正确的是( )
| A. | PH3比NH3稳定 | |
| B. | S2-半径比Cl-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na强 | |
| D. | 把钾放入氯化钠的水溶液中可制得金属钠 |

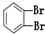 ⑨235U ⑩
⑨235U ⑩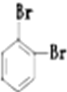
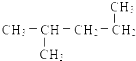 ⑫
⑫