题目内容
(16分)
根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
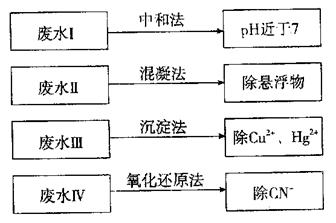
(1)①废水I若采用CO2处理,离子方程式是 。
②废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO-3)越大,净水效果越好,这是因为 。
③废水III中的汞元素存在如下转化(在空格上填相应的化学式):
Hg2++ =====CH3Hg++H+
我国规定,Hg2+的排放标准不能超过0.05 mg/L。若某工厂排放的废水1 L中含 Hg2+3×10-17mo1,是否达到了排放标准 (填“是”或“否”)。
④废水Ⅳ常用C12氧化CN-成CO2和N2,若参加反应的C12与CN-的物质的量之比为5:2,则该反应的离子方程式为 。
(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化刹的量,换算成氧的含量(以mg/L计)。某 研究性学习小组测定某水样的化学需氧量(COD),过程如下:
研究性学习小组测定某水样的化学需氧量(COD),过程如下:
I.取V1mL水样于锥形瓶,加入10.00 mL 0.2500 mol/L K2Cr2O7溶液。
II.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
III.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定。终点时消耗硫酸亚铁铵溶液V2 mL。
①I中,量取K2Cr20,溶液的仪器是 。
②Ⅱ中,碎瓷片的作用是 。
③III中,发生的反应为:Cr2O2-7+6Fe2++14 H+==2Cr3++6Fe3+7H2O
由此可知,该水样的化学需氧量COD= (用含c、V1、V2的表达式表示)。
根据废水中所含有害物质的不同,工业上有多种废水的处理方法。

(1)①废水I若采用CO2处理,离子方程式是 。
②废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO-3)越大,净水效果越好,这是因为 。
③废水III中的汞元素存在如下转化(在空格上填相应的化学式):
Hg2++ =====CH3Hg++H+
我国规定,Hg2+的排放标准不能超过0.05 mg/L。若某工厂排放的废水1 L中含 Hg2+3×10-17mo1,是否达到了排放标准 (填“是”或“否”)。
④废水Ⅳ常用C12氧化CN-成CO2和N2,若参加反应的C12与CN-的物质的量之比为5:2,则该反应的离子方程式为 。
(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化刹的量,换算成氧的含量(以mg/L计)。某
 研究性学习小组测定某水样的化学需氧量(COD),过程如下:
研究性学习小组测定某水样的化学需氧量(COD),过程如下:I.取V1mL水样于锥形瓶,加入10.00 mL 0.2500 mol/L K2Cr2O7溶液。
II.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
III.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定。终点时消耗硫酸亚铁铵溶液V2 mL。
①I中,量取K2Cr20,溶液的仪器是 。
②Ⅱ中,碎瓷片的作用是 。
③III中,发生的反应为:Cr2O2-7+6Fe2++14 H+==2Cr3++6Fe3+7H2O
由此可知,该水样的化学需氧量COD= (用含c、V1、V2的表达式表示)。
(1)①OH-+CO2
②HCO3-会促进Al3+的水解,生成更多的Al(OH)3,净水效果增强(2分)
③CH4(2分) 否(2分)
④4Cl2+2CN-+4H2O
(2)①酸式滴定管(或移液管)(2分)
②防止暴沸(2分)
③8000(15-cV2)/V1(2分)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
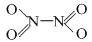 ,分子为平面结构。N2O4分子中N原子的杂化方式为 ▲ ,在N2O4分子的结构式上,将你认为是配位键的共价键上加上箭头 ▲ 。
,分子为平面结构。N2O4分子中N原子的杂化方式为 ▲ ,在N2O4分子的结构式上,将你认为是配位键的共价键上加上箭头 ▲ 。 O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式 。
O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式 。
 N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)="0.030" mol/L,则c(N2O4)= (保留两位有效数字);
N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)="0.030" mol/L,则c(N2O4)= (保留两位有效数字);

 积极推
积极推 行“限塑令”,加快研发利用二氧化碳合成的
行“限塑令”,加快研发利用二氧化碳合成的 聚碳酸酯类可降解塑料, 利于发展低碳经济、循环经济
聚碳酸酯类可降解塑料, 利于发展低碳经济、循环经济