题目内容
15.把VL含(NH4)2SO4和NH4Cl的混合溶液分为两等份,一份加入a mol烧碱并加热,恰好把全部NH3赶出;另一份加入含b mol BaCl2的溶液,使沉淀反应刚好完全.原溶液中Cl-的物质的量浓度(mol/L)为( )| A. | (2a-b)/V | B. | (2a-4b)/V | C. | (b-2a)/V | D. | (a-4b)/V |
分析 (NH4)2SO4和NH4Cl的混合溶液中加入amol烧碱加热,恰好使全部NH4+转化为氨气逸出,消耗的氢氧化钠中钠离子的物质的量就等于铵离子的物质的量;氯化钡与硫酸反应,钡离子的物质的量就等于硫酸根离子的物质的量,据此可以计算出硫酸铵的物质的量,再根据总的铵离子的物质的量计算出NH4Cl的物质的量,最后根据c=$\frac{n}{V}$计算出溶液中氯离子的物质的量浓度,注意带入的溶液的体积$\frac{V}{2}$L.
解答 解:溶液加入分为两等份,每份的体积为V=$\frac{V}{2}$L,一份bmol烧碱加热,恰好使全部NH4+转化为氨气逸出,反应生成了硫酸钠和NaCl,所以钠离子的物质的量就等于铵离子的物质的量,即:n(NH4+)=n(Na+)=amol;
另一份与含bmol BaCl2的溶液恰好反应,说明硫酸根离子的物质的量为bmol,硫酸铵中的铵离子的物质的量为2b,
所以NH4Cl的物质的量为:(a-2b)mol,NH4Cl的物质的量浓度为:c=$\frac{a-2b}{\frac{V}{2}}$=$\frac{2a-4b}{V}$mol/L,
c(Cl-)=c(NH4Cl)=$\frac{2a-4b}{V}$mol/L,
故选B.
点评 本题考查混合物反应的计算,题目难度中等,注意掌握物质的量浓度的概念及计算方法,计算浓度时注意每份溶液的体积为$\frac{V}{2}$L,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,下列有关说法正确的是( )
| A. | 丙烷分子中三个碳原子在一条直线上 | |
| B. | 符合通式CnH2n+2的均属于烷烃 | |
| C. | 丙烷的二氯代物有5种 | |
| D. | 丁烷能与氯气在光照时发生加成反应 |
10.NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A. | 1mol乙烯与乙醇的混合物在氧气中充分燃烧,消耗氧气的分子数为一定为3NA | |
| B. | 28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 0.1mol乙烷分子中含有的共价键数目为0.7NA | |
| D. | 在标准状态下,2.24L己烷含有的氢原子数目为1.4NA |
20.化学用语是学习化学的重要工具.下列用来表示物质变化的化学用语中,错误的是( )
| A. | 钢铁腐蚀时可能发生的正极反应:2H2O+O2+4e-═4OH- | |
| B. | 明矾水解的离子方程式:Al3++3 H2O?Al(OH)3+3H+ | |
| C. | 少量氢氧化钙溶液与碳酸氢钠溶液混合:OH-+HCO3-═H2O+CO32- | |
| D. | 表示氢气燃烧的热化学方程式2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ•mol-1 |
7.在周期表中,同一主族元素化学性质相似.但是也发现有些元素的化学性质和它在周期表左上方或右下角的另一主族元素性质相似,这称为对角线规则.下列有关锂及其化合物的叙述中正确的是( )
①锂单质跟钠单质的保存方法一样,均可保存在煤油中
②金属锂在空气中燃烧时,生成Li2O
③氢氧化锂的碱性比氢氧化铷弱.
①锂单质跟钠单质的保存方法一样,均可保存在煤油中
②金属锂在空气中燃烧时,生成Li2O
③氢氧化锂的碱性比氢氧化铷弱.
| A. | ①② | B. | ①③ | C. | ①②③ | D. | ②③ |
4.L一多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下: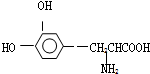 这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
 这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )| A. | 该有机物可看作氨基酸,也可看作是酚类物质 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 分子中至少有7个碳原子在同一平面内 | |
| D. | 既能与溴水发生取代反应,又能与溴水发生加成反应 |



