题目内容
(7分)为了探究HClO的漂白性,某同学设计了如下的实验。

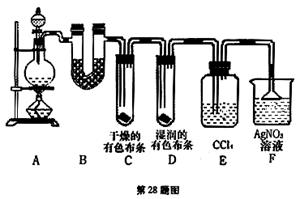
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是 ;从集气瓶B中湿润的红色布条的现象可得出的结论是 ,其中发生的反应的化学方程式为 。
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是 。
(3)烧杯中溶液所起的作用是 ,烧杯中所发生反应的化学方程式为 。
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2 mol·L—1的NaOH溶液的体积至少应为__________mL。

(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是 ;从集气瓶B中湿润的红色布条的现象可得出的结论是 ,其中发生的反应的化学方程式为 。
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是 。
(3)烧杯中溶液所起的作用是 ,烧杯中所发生反应的化学方程式为 。
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2 mol·L—1的NaOH溶液的体积至少应为__________mL。
(1) 干燥的Cl2没有漂白性, 氯水有漂白性 Cl2+ H2O="HCl+" HClO。
(2) 验证HCl是否有漂白性
(3) 吸收多余的Cl2, Cl2+2NaOH="NaCl+" NaClO+H2O 。 (4)200ml
(2) 验证HCl是否有漂白性
(3) 吸收多余的Cl2, Cl2+2NaOH="NaCl+" NaClO+H2O 。 (4)200ml
(1)干燥放热有色布条不褪色,说明干燥的Cl2没有漂白性。B中湿润的红色布条褪色,则说明氯水有漂白性,这是由于氯气溶于水生成次氯酸具有氧化性,反应式为Cl2+ H2O="HCl+" HClO。
(2)由于氯气和水反应,还生成氯化氢,所以还必须验证HCl是否有漂白性。
(3)氯气有毒,所以必须进行尾气处理,所以氢氧化钠是吸收多余的氯气的,方程式为Cl2+2NaOH="NaCl+" NaClO+H2O。
(4)4分钟内通过的氯气是1.12L×4=4.48L,物质的量为0.2mol,消耗氢氧化钠是0.4mol,所以氢氧化钠溶液的体积至少应是0.4mol÷2mol/L=0.2L。
(2)由于氯气和水反应,还生成氯化氢,所以还必须验证HCl是否有漂白性。
(3)氯气有毒,所以必须进行尾气处理,所以氢氧化钠是吸收多余的氯气的,方程式为Cl2+2NaOH="NaCl+" NaClO+H2O。
(4)4分钟内通过的氯气是1.12L×4=4.48L,物质的量为0.2mol,消耗氢氧化钠是0.4mol,所以氢氧化钠溶液的体积至少应是0.4mol÷2mol/L=0.2L。

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目