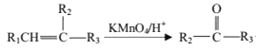题目内容
【题目】硫代硫酸钠俗称大苏打,是一种重要的化工产品,某兴趣小组设计以下装置(部分夹持装置省略)制备硫代硫酸钠晶体(Na2S2O3·5H2O):
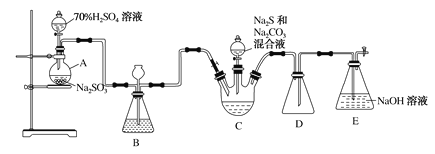
回答下列问题:
(1)仪器A的名称是____________,装置D的作用是____________。
(2)装置C中反应生成Na2S2O3和CO2,用化学方程式表示该反应________。
(3)以下实验步骤最合理的顺序是________(填序号)。
①按图示往各仪器中加入试剂
②打开C中分液漏斗旋塞,向三颈烧瓶内加入Na2S与Na2CO3的混合溶液
③连接装置并检查装置气密性
④向A中滴加70% H2SO4溶液
⑤取出C中混合物,经一系列操作得到产品
(4)装置E为尾气吸收装置,实验结束后装置E中的溶质有NaOH、Na2CO3、Na2SO3,还可能有________(填化学式),设计实验证明该物质的存在________。
【答案】圆底烧瓶 安全瓶,防倒吸 2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2 ③①④②⑤ Na2SO4 取实验结束后装置E中的溶液,滴加足量稀盐酸,然后再加入足量的BaCl2溶液,有白色沉淀生成,则可以确定含有Na2SO4
【解析】
浓硫酸和亚硫酸钠反应生成二氧化硫,通过B装置控制二氧化硫的生成速率,C中二氧化硫、硫化钠、碳酸钠反应生成硫代硫酸钠,D为安全瓶,防倒吸,二氧化硫有毒不能直接排空,E用碱液吸收尾气,据此解答。
(1)根据仪器构造可知仪器A的名称是圆底烧瓶;由于二氧化硫易溶于水,则装置D的作用是安全瓶,防倒吸。
(2)SO2、Na2S与Na2CO3反应生成Na2S2O3,根据原子守恒可知反应中还有二氧化碳生成,则装置C中反应生成Na2S2O3和CO2的化学方程式可表示为2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。
(3)根据实验原理可知首先是③连接装置并检查装置气密性,①按图示往各仪器中加入试剂,然后利用二氧化硫排尽装置中空气,即④向A中滴加70% H2SO4溶液,②打开C中分液漏斗旋塞,向三颈烧瓶内加入Na2S与Na2CO3的混合溶液,最后⑤取出C中混合物,经一系列操作得到产品,所以实验步骤最合理的顺序是③①④②⑤。
(4)装置E为尾气吸收装置,实验结束后装置E中的溶质有NaOH、Na2CO3、Na2SO3,由于亚硫酸钠易被氧化生成硫酸钠,则还可能有Na2SO4。又因为碳酸钠和亚硫酸钠会干扰硫酸根的检验,则实验证明该物质的存在的实验方案是取实验结束后装置E中的溶液,滴加足量稀盐酸,然后再加入足量的BaCl2溶液,有白色沉淀生成,则可以确定含有Na2SO4。

【题目】有机物 W 在医药和新材料等领域有广泛应用。W 的一种合成路线如图:
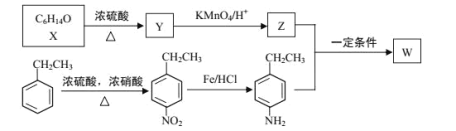
已知部分信息如下:
① | 1molY完全反应生成2molZ,且在加热条件下Z不能和新制氢氧化铜悬浊液反应 |
② |
|
③ | RCH2NH2+ |
请回答下列问题:
(1)Y 的化学名称是___;Z 中官能团的名称是___;
(2)![]() 中_____________(填“有”或“无”)手性碳原子;图示中 X 转化为 Y 的反应类型是___。
中_____________(填“有”或“无”)手性碳原子;图示中 X 转化为 Y 的反应类型是___。
(3)生成 W 的化学方程式为___。
(4)G 是对硝基乙苯的同分异构体,G 能和碳酸钠反应产生气体且分子中含有—NH2(氨基),G的同分异构体有___种(不考虑立体结构),其中在核磁共振氢谱上峰的面积比为 1∶2∶2∶2∶2 的结构简式为_________________。
(5)设计以苯乙烯和丙酮为原料制备药物中间体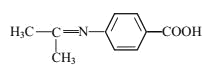 的合成路线__________(无机试剂自选)。
的合成路线__________(无机试剂自选)。
【题目】X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是

X | Y | Z | W | |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
A. AB. BC. CD. D