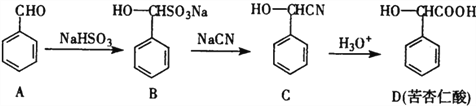
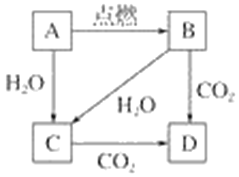
题目内容
【题目】[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
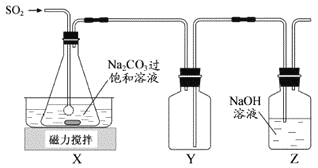
当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为
2NaHSO3===Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为____________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。
【答案】(1)2SO2+CO32-+H2O=2HSO3-+CO2 (2)防止倒吸 (3)①抽滤瓶;②减少Na2S2O5的在水中的溶解;
(4)在制备过程中Na2S2O5分解生成生Na2SO3,Na2SO3被氧化生成Na2SO4。
【解析】试题在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,发生反应生成NaHSO3和CO2,多余的二氧化硫可用氢氧化钠溶液吸收,因二氧化硫易溶于氢氧化钠溶液,Y为安全瓶,可防止倒吸。
(1)向Na2CO3过饱和溶液中通入SO2,发生反应生成NaHSO3和CO2,反应的离子方程式为2SO2+CO32-+H2O=2HSO3-+CO2,故答案为:2SO2+CO32-+H2O=2HSO3-+CO2;
(2)二氧化硫易溶于氢氧化钠溶液,Y为安全瓶,可防止倒吸,故答案为:防止倒吸;
(3)①组成减压抽滤装置的主要仪器是布氏漏斗、吸滤瓶和抽气泵,故答案为:吸滤瓶;②由反应2NaHSO3═Na2S2O5+H2O可知,增大HSO3-的浓度,有利于生成Na2S2O5,用饱和SO2水溶液洗涤,可降低Na2S2O5的溶解度,减少Na2S2O5的溶解,故答案为:减少Na2S2O5在水中的溶解;
(4)Na2S2O5易分解生成Na2SO3,且Na2SO3易被氧化,可知验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,故答案为:在制备过程中Na2S2O5易分解生成Na2SO3,且Na2SO3易被氧化生成Na2SO4。