题目内容
【题目】下列说法不正确的是
A. 已知冰的熔化热为6.0kJ·mol-1,冰中氢键键能为20kJmol-1,假设每摩尔冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键
B. 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a,Ka=(ca)2/c(1-a)。若加水稀释,,则CH3COOH![]() CH3COO-+H+向右移动,a增大,Ka不变
CH3COO-+H+向右移动,a增大,Ka不变
C. 甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
D. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
【答案】D
【解析】试题分析: A.冰是由水分子通过氢键形成的分子晶体,冰的熔化热为6.0kJmol-1,1mol冰变成0℃的液态水所需吸收的热量为6.0kJ,全用于打破冰的氢键,冰中氢键键能为20.0kJmol-1,1mol冰中含有2mol氢键,需吸收40.0kJ的热量.6.0kJ/40.0kJ×100%=15%.由计算可知,最多只能打破1mol冰中全部氢键的15%,故A正确;B.Ka是电离常数,是弱电解质达电离平衡时的平衡常数,在一定温度下,与浓度无关.Ka的计算用溶液中电离出来的各离子浓度乘积与溶液中未电离的电解质分子浓度的比值,一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,CH3COOHCH3COO-+H+醋酸电离出的CH3COO-和H+浓度均为cα,溶液中未电离的电解质分子浓度为c(1-α),故题中Ka=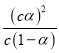 。若加入少量醋酸钠固体,CH3COONa ═ CH3COO- + Na+增大了CH3COO-的浓度,CH3COOHCH3COO-+H+向左移动,α减小,但醋酸的浓度比原先的大,分子分母中c变大,Ka不变,故B正确;C、甲烷燃烧的热化学方程式中的产物都是稳定状态,符合燃烧热的概念,故C正确;D、反应是可逆反应,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),不能进行完全,反应的焓变是对应化学方程式物质全部反应时放出的热量,故D错误;故选D。
。若加入少量醋酸钠固体,CH3COONa ═ CH3COO- + Na+增大了CH3COO-的浓度,CH3COOHCH3COO-+H+向左移动,α减小,但醋酸的浓度比原先的大,分子分母中c变大,Ka不变,故B正确;C、甲烷燃烧的热化学方程式中的产物都是稳定状态,符合燃烧热的概念,故C正确;D、反应是可逆反应,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),不能进行完全,反应的焓变是对应化学方程式物质全部反应时放出的热量,故D错误;故选D。

【题目】仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置就能实现相应实验目的是( )
选项 | 实验目的 | 实验仪器或装置 |
A | 除去KCl中少的 MnO2 | 烧杯、玻璃棒、分液漏斗 |
B | 用10mol/L的盐酸配制100mL0.1mol/L的盐酸 | 100mL容量瓶、玻璃棒、烧杯 |
C | 用氯化钠溶液制备氯化钠晶体 |
|
D | 用右图装置验证SO2的漂白性 |
|
A. A B. B C. C D. D