题目内容
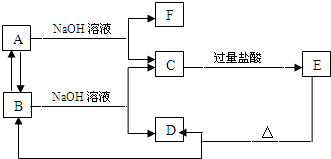
以下各单质和化合物之间存在如图所示的转化关系:
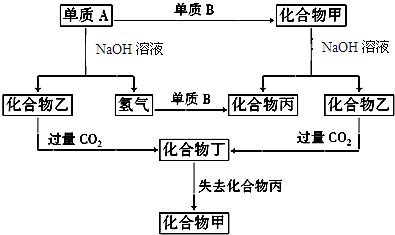
若单质A为非金属:
(1)试确定A、B和乙的化学式:A______,B______,乙______.
(2)写出化合物甲与NaOH溶液反应的化学方程式______.
若单质A为金属:
(3)写出A生成化合物乙的离子方程式______
(4)写出化合物乙与过量CO2反应的化学方程式______
(5)写出化合物丁失去化合物丙的化学方程式______.

若单质A为非金属:
(1)试确定A、B和乙的化学式:A______,B______,乙______.
(2)写出化合物甲与NaOH溶液反应的化学方程式______.
若单质A为金属:
(3)写出A生成化合物乙的离子方程式______
(4)写出化合物乙与过量CO2反应的化学方程式______
(5)写出化合物丁失去化合物丙的化学方程式______.
若单质A为非金属:应为Si,Si和NaOH溶液反应生成Na2SiO3和H2,所以乙是Na2SiO3,Na2SiO3溶液与过量二氧化碳反应生成H2SiO3,即化合物丁为H2SiO3,可失去水生成SiO2,则化合物丙为H2O,化合物甲为SiO2,单质B为O2,
(1)通过以上分析知,A为Si,B为O2,乙为Na2SiO3,故答案为:Si;O2;Na2SiO3;
(2)二氧化硅与氢氧化钠反应生成硅酸钠和水,反应的方程式为SiO2+2NaOH═Na2SiO3+H2O,故答案为:SiO2+2NaOH═Na2SiO3+H2O;
当A是金属时,应为Al,Al和NaOH溶液反应生成NaAlO2和H2,则乙是NaAlO2,NaAlO2溶液与过量二氧化碳反应生成Al(OH)3,即化合物丁为Al(OH)3,失去水可生成Al2O3,也可与氢氧化钠反应,则化合物丙为H2O,化合物甲为Al2O3,单质B为O2,
(3)铝可与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)偏铝酸钠与过量二氧化碳反应生成氢氧化铝和碳酸氢钠,反应的方程式为NaAlO2+CO2+2H2O═Al(OH)3↓+NaHCO3,
故答案为:NaAlO2+CO2+2H2O═Al(OH)3↓+NaHCO3;
(5)氢氧化铝可加热分解生成氧化铝,反应的方程式为2Al(OH)3
Al2O3+3H2O,故答案为:2Al(OH)3
Al2O3+3H2O.
(1)通过以上分析知,A为Si,B为O2,乙为Na2SiO3,故答案为:Si;O2;Na2SiO3;
(2)二氧化硅与氢氧化钠反应生成硅酸钠和水,反应的方程式为SiO2+2NaOH═Na2SiO3+H2O,故答案为:SiO2+2NaOH═Na2SiO3+H2O;
当A是金属时,应为Al,Al和NaOH溶液反应生成NaAlO2和H2,则乙是NaAlO2,NaAlO2溶液与过量二氧化碳反应生成Al(OH)3,即化合物丁为Al(OH)3,失去水可生成Al2O3,也可与氢氧化钠反应,则化合物丙为H2O,化合物甲为Al2O3,单质B为O2,
(3)铝可与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)偏铝酸钠与过量二氧化碳反应生成氢氧化铝和碳酸氢钠,反应的方程式为NaAlO2+CO2+2H2O═Al(OH)3↓+NaHCO3,
故答案为:NaAlO2+CO2+2H2O═Al(OH)3↓+NaHCO3;
(5)氢氧化铝可加热分解生成氧化铝,反应的方程式为2Al(OH)3
| ||
| ||

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 C:____________;
C:____________;