题目内容
未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机,这类材料中被研究得较多的是化合物G.
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y.G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl.请推断:①化合物G的化学式为______,②由1mol NH3和0.75mol E恰好完全反应,化合物E的分子式为______.
(2)粉末状G能够与空气中的氧气和水反应,所得的产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料.与氧气反应所得的产物还有一种单质;与水反应生成的另一种产物是该种单质元素的氢化物.请写出化合物G与水反应的化学方程式:______.
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表达为Si6-xAlxOxN8-x.在接近1700℃时x的极限值约为4.0,在1400℃时x为2.0,以保持整个化合物呈电中性.则赛伦中各元素的化合价为Si______、Al______、O______、N______.
解:(1)生产玻璃的主要原料为二氧化硅、大理石、碳酸钠,其中是酸性氧化物的只有二氧化硅,即粉末A与水反应生成二氧化硅和氨气,则A中必含硅元素和氮元素,由G的相对分子质量及Si、N的质量分数,可知:n(Si):n(N)=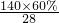 :
: =3:4,则G的化学式为Si3N4,
=3:4,则G的化学式为Si3N4,
由E与NH3的复分解反应,可知E中含有Si和Cl两种元素,再据NH3与E的反应及二者的物质的量的关系1mol NH3和0.75molE恰好完全反应,可求出E的化学式为SiCl4.
故答案为:Si3N4;SiCl4;
(2)由题意可知粉末状G能够与空气中的氧气和水反应,所得的产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料,应生成SiO2,另一种氢化物为NH3,则与水反应的方程式为Si3N4+6H2O=3SiO2+4NH3,故答案为:Si3N4+6H2O=3SiO2+4NH3;
(3)当x=4.0时,化学式为Si2Al4O4N4,当x=2.0时,化学式为Si4Al2O2N6,不管是用x=4.0计算,还是用x=2.0计算,N的化合价都为-3价,O的化合价为-2价,根据化合价代数和为0可知Si为+4价,Al为+3价,由物理性质可知应为原子晶体,故答案为:+4;+3;-2;-3;原子晶体.
分析:(1)由G的相对分子质量及Si、N的质量分数,可以求出G的化学式为Si3N4;由E与NH3的复分解反应,可知E中含有Si和Cl两种元素,再据NH3与E的反应及二者的物质的量的关系,可求出E的化学式为SiCl4;
(2)根据产物和质量守恒定律分析出G中含有的元素,继而书写并配平化学方程式;
(3)根据化合价代数和为0的原则判断.
点评:本题考查无机物的推断,题目难度中等,注意根据物质的性质以及发生的反应现象判断物质的组成,答题中注意不要忽视物质的用途.
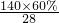 :
: =3:4,则G的化学式为Si3N4,
=3:4,则G的化学式为Si3N4,由E与NH3的复分解反应,可知E中含有Si和Cl两种元素,再据NH3与E的反应及二者的物质的量的关系1mol NH3和0.75molE恰好完全反应,可求出E的化学式为SiCl4.
故答案为:Si3N4;SiCl4;
(2)由题意可知粉末状G能够与空气中的氧气和水反应,所得的产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料,应生成SiO2,另一种氢化物为NH3,则与水反应的方程式为Si3N4+6H2O=3SiO2+4NH3,故答案为:Si3N4+6H2O=3SiO2+4NH3;
(3)当x=4.0时,化学式为Si2Al4O4N4,当x=2.0时,化学式为Si4Al2O2N6,不管是用x=4.0计算,还是用x=2.0计算,N的化合价都为-3价,O的化合价为-2价,根据化合价代数和为0可知Si为+4价,Al为+3价,由物理性质可知应为原子晶体,故答案为:+4;+3;-2;-3;原子晶体.
分析:(1)由G的相对分子质量及Si、N的质量分数,可以求出G的化学式为Si3N4;由E与NH3的复分解反应,可知E中含有Si和Cl两种元素,再据NH3与E的反应及二者的物质的量的关系,可求出E的化学式为SiCl4;
(2)根据产物和质量守恒定律分析出G中含有的元素,继而书写并配平化学方程式;
(3)根据化合价代数和为0的原则判断.
点评:本题考查无机物的推断,题目难度中等,注意根据物质的性质以及发生的反应现象判断物质的组成,答题中注意不要忽视物质的用途.

练习册系列答案
相关题目
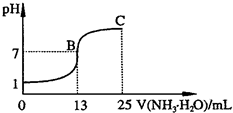 (2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.
(2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.