题目内容
 (2009?揭阳二模)如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为2Na2S2+NaBr3
(2009?揭阳二模)如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为2Na2S2+NaBr3| 放电 |
| 充电 |
分析:根据电池充、放电的化学反应方程式为2Na2S2+NaBr3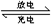 Na2S4+3NaBr可知,放电时为原电池反应:负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr;
Na2S4+3NaBr可知,放电时为原电池反应:负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr;
充电时为电解池反应:阳极电极反应为:3NaBr-2e-=NaBr3+2Na+;阴极电极反应为:2Na++Na2S4+2e-=2Na2S2;
阳极原电池原理和电极原理分析判断;
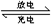 Na2S4+3NaBr可知,放电时为原电池反应:负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr;
Na2S4+3NaBr可知,放电时为原电池反应:负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr;充电时为电解池反应:阳极电极反应为:3NaBr-2e-=NaBr3+2Na+;阴极电极反应为:2Na++Na2S4+2e-=2Na2S2;
阳极原电池原理和电极原理分析判断;
解答:解:A、有0.1molNa+通过离子交换膜,说明有0.1mol电子转移,故A正确;
B、电池放电时,正极反应为得到电子发生的还原反应,正极反应为:NaBr3+2Na++2e-=3NaBr,故B错误;
C、依据图示方向,电极反应,充电过程中钠离子从左到右通过离子交换膜,故C错误;
D、依据原电池电极反应分析,放电过程中钠离子从右到左通过离子交换膜,故D正确;
故选AD.
B、电池放电时,正极反应为得到电子发生的还原反应,正极反应为:NaBr3+2Na++2e-=3NaBr,故B错误;
C、依据图示方向,电极反应,充电过程中钠离子从左到右通过离子交换膜,故C错误;
D、依据原电池电极反应分析,放电过程中钠离子从右到左通过离子交换膜,故D正确;
故选AD.
点评:本题考查了原电池和电解池的工作原理应用,电极反应电极判断是解题关键,题目难度中等.

练习册系列答案
相关题目
 (2009?揭阳二模)如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
(2009?揭阳二模)如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )