��Ŀ����
����Ŀ�����������ʣ���Cl2��KCl��NaHCO3��ŨH2SO4��NH3��Al��OH��3������������
��1��ֻ�����Ӽ����ɵ���_______��
��2���д̼�����ζ������ʹ��̪��Һ������_______��
��3�����³�ѹ�³ʻ���ɫ��������_______��
��4��ʵ���ҳ��������������_______��
��5����ǿ���ǿ����Һ���ܷ�����Ӧ����û�������������_______��
��6����ѧ���ʲ��ȶ�����һ���������ֽ������������ʵ���_______��
���𰸡��ڢݢ٢ܢޢ�
��������
��1��ֻ�����Ӽ�����˵���������ɼ������Ӻͼ������ӹ��ɣ���ԭ�����γɵ����ӣ�KCl��ֻ�����ӹ��ɵ����ʣ���Ϊ�ڣ�
��2���̼�����ζ������ʹ��̪��Һ�����Ǽ������壬Ӧ����NH3����Ϊ�ݣ�
��3�������ǻ���ɫ���壬��Ϊ�٣�
��4��Ũ���������ˮ�Կ��Ը������壬��Ϊ�ܣ�
��5����ǿ���ǿ����Һ���ܷ�����Ӧ����û�������������������������������������ǿ���ǿ�Ӧ�ķ���ʽΪAl��OH��3+3H+��Al3++3H2O��Al��OH��3+OH��=AlO2��+2H2O����Ϊ�ޣ�
��6 ����ѧ���ʲ��ȶ�����һ���������ֽ������������ʵ���̼�����ƣ�����ʽΪ2NaHCO3![]() Na2CO3+H2O+CO2���������������ȷֽ�������������ˮ�������ʣ������������Ⱥ��ѷֽ⣬��Ϊ�ۡ�
Na2CO3+H2O+CO2���������������ȷֽ�������������ˮ�������ʣ������������Ⱥ��ѷֽ⣬��Ϊ�ۡ�

����Ŀ��ˮ�ϼ�ʽ̼��þ[4MgCO3��Mg(OH)2��4H2O],�ֳ�����̼��þ����������þ������������Ϊ̼��þ90%,̼���10%��̼������ȡ��

��1���������б�������,ѡ��������Ӧ������¶�__________;������___________________________��
�����¶�/�� | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
ת����/% | 50.3 | 58.2 | 85.1 | 85.2 | 90.7 | 91.2 | 91.5 |
��2��̼����Ӧ������Mg(HCO3)2,����Mg(HCO3)2�Ļ�ѧ����ʽΪ____________��
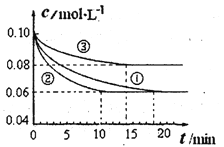
��3������ͼ��__________��__________����Ϊ̼����Ӧ�ṩ������̼Դ��
��4���й����������±ˮ̼������ȡ����̼��þ��
��±ˮ�к���Fe2+��Mn2+,����Ũ��С��1��10-5mol��L-1ʱ,������Ϊ��ȫ��ȥ������ʱ��������ҺPHΪ9.5ʱ,��ʱMn2+С��__________mol��L-1,�������������
���� | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
Ksp | 10-11 | 10-39 | 10-17 | 10-14 |
�������Fe2+ת��ΪFe3+,�ӻ����Ƕ�ѡ������ʵ�������Ϊ__________��
A��Ca(ClO)2 B��Cl2 C��H2O2 D��HNO3
�����з�����,�Ϻõ�Ϊ__________��������______________________��
![]()
����Ŀ������(H2C2O4)��Һ������KMnO4��Һ��Ӧʱ����Һ��ɫ����������죬ijѧϰС��̽����Ӧ������ʹ��ɫ�ӿ����Ҫԭ��������:
���������ϡ�KMnO4��Һ����H2C2O4�ķ�Ӧ����Ϊ��
![]()
��������衿����1:�÷�ӦΪ���ȷ�Ӧ
����2:��Ӧ���ɵ�Mn2���Ը÷�Ӧ�д�����
����3:K���Ը÷�Ӧ�д�����
��С��ͬѧδ���Ũ��ʹ��Ӧ���ʼӿ�ļ��裬ԭ���� ��
����ơ����ʵ�顿��1����ȡ g���ᾧ��(H2C2O4��2H2O)������500 mL 0.10 mol/L H2C2O4��Һ��
�������������б����õ���2�ֶ���������������ƽ�� ��
�����в�����ʹ������ҺŨ��ƫ�͵��� (������ѡ�����ĸ���)��
A����ȡ���ᾧ��ʱ�������ᾧ�����������ƽ���� |
B������ʱ���ӿ̶��� |
C�����ձ�����Һת�Ƶ�����ƿ֮ǰ������ƿ������������ˮ |
D��ҡ�Ⱥ�����ҺҺ����ڿ̶��ߣ������ý�ͷ�ιܼ�ˮ�ٶ��� |
��2�����̽������¼����
ʵ�� | �ձ��������Լ�������(mL) | �������� | ��Һ��ɫʱ��(s) | |||
0.10 mol/L | ��Ũ�� | H2O | 0.50 mol/L | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | ˮԡ�����¶�65 �� | 15 |
3 | 30 | 20 | 30 | 20 | ��������MnSO4���� | 3.6 |
4 | 30 | 20 | x | 20 | ����5 mL 0.10 mol/LK2SO4��Һ | 18 |
��x = ������2����
��3������KMnO4������ˮ���л�������أ�Ϊ���ƺ��ȶ���KMnO4��Һ����Ũ����궨��ȡ10.00 mL 0.10 mol/L H2C2O4��Һ����ƿ�У�����10 mL 0.50 mol/Lϡ���ᣬ�ã�2����KMnO4��Һ�ζ�����ƿ��ǡ�ó�dz��ɫ���Ұ���Ӳ���ɫ����¼���ݣ�ƽ������ʵ�飬ƽ������KMnO4��Һ40.00 mL���������Һ������KMnO4��Һ��Ӧ�����ӷ���ʽΪ�� ������ʵ����KMnO4��Һ�����ʵ���Ũ��Ϊ ��