题目内容
15.2.5mol Ba(OH)2中含有2.5NA个Ba2+,含有5NA个OH-,2.5mol Ba(OH)2的质量是427.5g.含有1.204×1024个OH-的Ba(OH)2的物质的量是1mol.分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合物质的构成计算该题.
解答 解:2.5mol Ba(OH)2中含有2.5molBa2+,数目为2.5NA,含有5molOH-,数目为5NA,m(Ba(OH)2)=2.5mol×171g/mol=427.5g,
n(OH-)=$\frac{1.204×1{0}^{24}}{6.02×1{0}^{23}/mol}$=2mol,n(Ba(OH)2)=$\frac{1}{2}$=n(OH-)=1mol,
故答案为:2.5NA;5NA;427.5;1mol.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握公式的运用,难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
6.据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:HC≡C-C≡C-C≡C-C≡C-C≡N.对该物质判断正确的是( )
| A. | 该分子中不含极性共价键 | B. | 能使酸性高锰酸钾溶液褪色 | ||
| C. | 不能发生加成反应 | D. | 可由乙炔和含氮化合物加聚制得 |
3.2mol Cl2和2mol CO2相比较,下列叙述中正确的是( )
| A. | 分子数相等 | B. | 原子数相等 | C. | 质子数相等 | D. | 质量相等 |
9.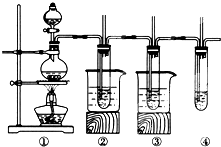 在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.
在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.
(1)③试管中制取次氯酸钠的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格.
(3)此实验有一个明显的不足之处,应如何改进?④后增加一个盛有氢氧化钠溶液的烧杯用于吸收多余的氯气.
 在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.
在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.(1)③试管中制取次氯酸钠的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格.
| 实验现象 | 原因 |
| 溶液最初从紫色变为红色 | 氯气与水反应生成的HCl使石蕊试液变红 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成HClO具有漂白性 |
| 最后溶液从无色逐渐变为浅黄绿色 | 过量氯气溶解于水中 |
10.具有下列价电子数的原子,最难形成离子的是( )
| A. | L层6个 | B. | L层4个 | C. | M层2个 | D. | M层7个 |
 .在工业上,用氯化钠为原料,在碱性溶液中,通过电解的方法可制得NaClO,用离子方程式表示制取NaClO的电解总反应:Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$ClO-+H2↑,将等浓度等体积的NaClO与Na2SO3溶液混合后,两者恰好完全反应,写出混合过程的离子反应方程式ClO-+SO32-=Cl-+SO42-.
.在工业上,用氯化钠为原料,在碱性溶液中,通过电解的方法可制得NaClO,用离子方程式表示制取NaClO的电解总反应:Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$ClO-+H2↑,将等浓度等体积的NaClO与Na2SO3溶液混合后,两者恰好完全反应,写出混合过程的离子反应方程式ClO-+SO32-=Cl-+SO42-.