题目内容
某课题小组同学测量液态奶含氮量的实验过程如下:
原理:液态奶 (NH4)2SO4溶液
(NH4)2SO4溶液 NH3
NH3 (NH4)2B4O7
(NH4)2B4O7
步骤: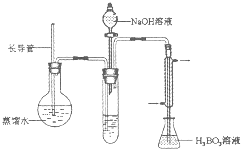
①在烧杯中加入10.00mL液态奶和辅助试剂,加热充分反应;
②将反应液转移到大试管中;
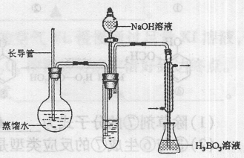
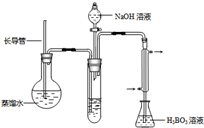
③按右图装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
⑤重复测定数次,再用10.00mL蒸馏水代替液态奶进行上述操作.
数据记录如下:
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积/mL |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 25.50 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 4 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 5 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 1.50 |
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的离子方程式为______.
(2)步骤③的实验装置中需要加热的仪器是______(填仪器名称),长导管的作用是______.
(3)不做空白对照实验对实验结果有何影响______(填“无影响”,或“偏高”,或“偏低”).
(4)计算10.00mL液态奶中的含氮量应代人计算的盐酸体积是______mL,该液态奶的含氮量______mg?mL-1.
解:(1)硼的化合价未变化,发生类似复分解反应,反应方程式为(NH4)2B4O7+2HCl+5H2O=4 H3BO3+2NH4Cl,反应的离子方程式为:B4O72-+2H++5H2O=4H3BO3;
故答案为:B4O72-+2H++5H2O=4H3BO3;
(2)加热圆底烧瓶产生水蒸气,进入试管中将生成的氨气吹出;加热产生水蒸气,装置内压强增加,长导管防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用,故答案为:圆底烧瓶;防止装置中压力过大而发生危险,防止冷却时发生倒吸,起到安全管的作用;
(3)对照使用目的是消除其他试剂、实验操作等因素引起的误差,不做空白对照实验,消耗的盐酸量增大,引起实验结果偏高,故答案为:偏高;
(4)盐酸的体积为33.45ml+33.55ml+33.50ml 3-1.5ml=32.00ml=0.03200L,令10ml该液态奶的含氮量的质量为mg,则
2N~(NH4)2B4O7~2HCl
28g 2mol
mg 0.03200L×0.1000mol/L
所以m=28g×0.03200ml×0.1000mol/L 2mol=0.04480g,
该液态奶的含氮量为 =4.480mg/ml;
=4.480mg/ml;
故答案为:32.00;4.480.
分析:(1)滴加盐酸(NH4)2B4O7转化为H3BO3,硼的化合价未变化,发生类似复分解反应,还有氯化铵生成;
(2)圆底烧瓶加热产生水蒸气,装置内压强增加,防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用;
(3)实验组与对照组的无关变量的影响是相等的,这样通过空白对照实验,对比实验的结果,排除无关变量的影响,则可认定为是来自实验变量的效果,使实验结果更有说服力;
(4)根据N元素守恒,及滴定反应找出N原子与HCl的关系式,根据关系式计算,注意盐酸的体积取3次滴定的平均值减去1.5ml(不含奶时消耗盐酸的体积为1.5ml).
点评:本题知识涉及元素化合物、实验原理、化学计算等,侧重考查学生对实验方案理解、元素化合物的知识,难度较大,易错点为计算液态奶的含氮量时盐酸体积应为3次滴定的平均值减去1.5ml(不含奶时消耗盐酸的体积为1.5ml).
故答案为:B4O72-+2H++5H2O=4H3BO3;
(2)加热圆底烧瓶产生水蒸气,进入试管中将生成的氨气吹出;加热产生水蒸气,装置内压强增加,长导管防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用,故答案为:圆底烧瓶;防止装置中压力过大而发生危险,防止冷却时发生倒吸,起到安全管的作用;
(3)对照使用目的是消除其他试剂、实验操作等因素引起的误差,不做空白对照实验,消耗的盐酸量增大,引起实验结果偏高,故答案为:偏高;
(4)盐酸的体积为33.45ml+33.55ml+33.50ml 3-1.5ml=32.00ml=0.03200L,令10ml该液态奶的含氮量的质量为mg,则
2N~(NH4)2B4O7~2HCl
28g 2mol
mg 0.03200L×0.1000mol/L
所以m=28g×0.03200ml×0.1000mol/L 2mol=0.04480g,
该液态奶的含氮量为
 =4.480mg/ml;
=4.480mg/ml;故答案为:32.00;4.480.
分析:(1)滴加盐酸(NH4)2B4O7转化为H3BO3,硼的化合价未变化,发生类似复分解反应,还有氯化铵生成;
(2)圆底烧瓶加热产生水蒸气,装置内压强增加,防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用;
(3)实验组与对照组的无关变量的影响是相等的,这样通过空白对照实验,对比实验的结果,排除无关变量的影响,则可认定为是来自实验变量的效果,使实验结果更有说服力;
(4)根据N元素守恒,及滴定反应找出N原子与HCl的关系式,根据关系式计算,注意盐酸的体积取3次滴定的平均值减去1.5ml(不含奶时消耗盐酸的体积为1.5ml).
点评:本题知识涉及元素化合物、实验原理、化学计算等,侧重考查学生对实验方案理解、元素化合物的知识,难度较大,易错点为计算液态奶的含氮量时盐酸体积应为3次滴定的平均值减去1.5ml(不含奶时消耗盐酸的体积为1.5ml).

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
I.(1)对下列仪器:
A.移液管 B.蒸馏烧瓶 C.滴定管 D.量筒
E.容量瓶 F.蒸发皿 G.分液漏斗 E.吸滤瓶
①使用时必须检查是否漏水的有______(填序号)
②使用前必须用待盛液润洗的有______(填序号)
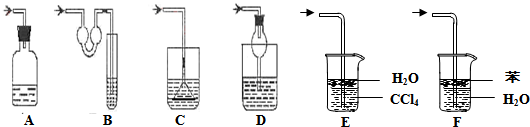
(2)如图各种尾气吸收装置中,适合于吸收NH3气体,而且能防止倒吸的有______.

Ⅱ.某课题小组同学测量液态奶含氮量的实验过程如下:
实验原理:
(NH4)2SO4溶液液态奶辅助试剂加热吹出NaOHNH3吸收H3BO3(NH4)2B4O7溶液用标准盐酸滴定
实验步骤:
①在烧杯中加入10.00mL液态奶和辅助试剂,加热充分反应;
②将反应液转移到大试管中;
③按如图装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
⑤重复测定两次,再用10.00mL蒸馏水代替液态奶进行上述操作.
数据记录如下:
回答下列问题:
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为______.
(2)步骤③的实验装置中需要加热的仪器是______(填仪器名称),长导管的作用是______.
(3)设计4号空白对照实验的目的是______.
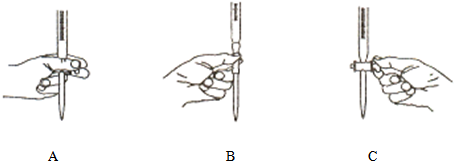
(4)本实验④中操作滴定管的以下图示中,正确的是______(填编号).

(5)计算该液态奶的含氮量为______mg?mL-1.(保留四位有效数字)

A.移液管 B.蒸馏烧瓶 C.滴定管 D.量筒
E.容量瓶 F.蒸发皿 G.分液漏斗 E.吸滤瓶
①使用时必须检查是否漏水的有______(填序号)
②使用前必须用待盛液润洗的有______(填序号)
(2)如图各种尾气吸收装置中,适合于吸收NH3气体,而且能防止倒吸的有______.

Ⅱ.某课题小组同学测量液态奶含氮量的实验过程如下:
实验原理:
(NH4)2SO4溶液液态奶辅助试剂加热吹出NaOHNH3吸收H3BO3(NH4)2B4O7溶液用标准盐酸滴定
实验步骤:
①在烧杯中加入10.00mL液态奶和辅助试剂,加热充分反应;
②将反应液转移到大试管中;
③按如图装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
⑤重复测定两次,再用10.00mL蒸馏水代替液态奶进行上述操作.
数据记录如下:
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50 |
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为______.
(2)步骤③的实验装置中需要加热的仪器是______(填仪器名称),长导管的作用是______.
(3)设计4号空白对照实验的目的是______.
(4)本实验④中操作滴定管的以下图示中,正确的是______(填编号).

(5)计算该液态奶的含氮量为______mg?mL-1.(保留四位有效数字)


 ④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;