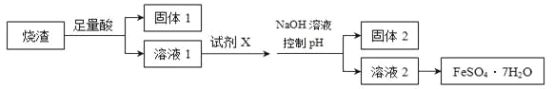
题目内容
【题目】如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内液面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中液面继续上升,经过多次重复后,试管内完全被充满,原来试管中盛装的气体是( ) 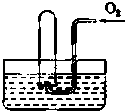
A.可能是N2和NO2的混合气体
B.一定是NO2气体
C.可能是NO和NO2的混合气体
D.只可能是NO2一种气体
【答案】C
【解析】解:A.当充入氧气后,NO2可在溶液中发生反应4NO2+O2+2H2O=4HNO3 , 但N2和水不反应且不溶于水,故最后有气体剩余,故试管内不能完全被水充满,故A不选;
B.O2与NO2可在溶液中发生反应4NO2+O2+2H2O=4HNO3 , 试管内能完全被水充满,可能是NO2一种气体,但不一定是,也可能为NO和NO2的混合气体,故B不选;
C.NO与NO2的混和气体,当向试管内鼓入氧气后,可在溶液中发生反应4NO+3O2+2H2O=4HNO3 , 4NO2+O2+2H2O=4HNO3 , 试管内能完全被水充满,可能是NO和NO2的混合气体,故C选;
D.当充入氧气后,NO2可在溶液中发生反应4NO2+O2+2H2O=4HNO3 , 二氧化氮能完全被水吸收无气体剩余,故试管内能被水完全充满,可能是NO2一种气体,但不是只可能,也可为NO和NO2的混合气体,故D不选;
故选C.
在氮的氧化物中通入氧气可被水完全吸收生成硝酸,有关反应为4NO+3O2+2H2O=4HNO3、4NO2+O2+2H2O=4HNO3 , 但氮气和水不反应且不溶于水,试管中盛装的是红棕色气体一定有NO2气体,可能含气体气体.

【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。请回答下列问题。
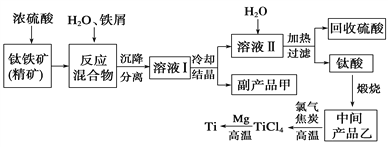
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C═2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为_______________;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为____________________。
(2)上述生产流程中加入铁屑的目的是_________________________,此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于_______时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为___________________________________________________________。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为________。Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是_________。除去所得金属钛中少量的金属镁可用的试剂是__________________。