题目内容
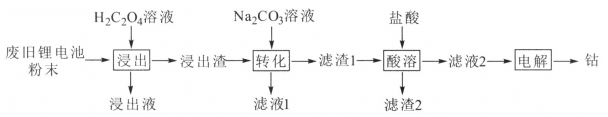
【题目】某废旧锂电池材料含有钴酸锂(LiCoO2)、导电剂石墨和铝粉等。回收废旧锂电池中钴的工艺流程如下:
已知:Ksp(CoC2O4)=6.0×10-8,Ksp(CoCO3)=1.5×10-13。
回答下列问题:
(1) LiCoO2中,Co元素的化合价为______________。
(2)“浸出液”的主要成分是LiHC2O4、Al(HC2O4)3,“浸出渣”的主要成分是CoC2O4。“浸出”中生成CoC2O4的化学方程式为__________,若H2C2O4用量过大,CoC2O4的产率反而会降低,原因是____。
(3)“转化”中加入Na2CO3溶液发生反应的离子方程式为______________,该反应进行的程度较大,试通过计算其平衡常数K并解释原因______________。
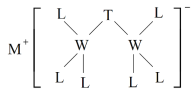
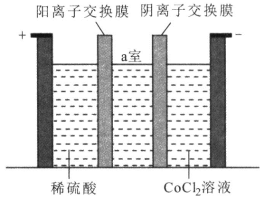
(4)“电解”时装置如图所示。阳极的电极反应式为_______,电解后a室中的电解液可返回工序继续使用。
(5)某废旧锂电池粉末中LiCoO2的质量分数为49%,将50吨该废料进行回收利用,电解得到钴5.9吨,则钴的回收率为_____________。
【答案】+3 2LiCoO2+5H2C2O4=2LiHC2O4+2CoC2O4+4H2O+2CO2↑ CoC2O4与过量的H2C2O4反应转化成Co(HC2O4)2而溶解 CoC2O4(s)+ CO32-(aq)![]() CoCO3(s) + C2O42-(aq) 该反应的平衡常数K=
CoCO3(s) + C2O42-(aq) 该反应的平衡常数K=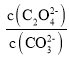 =
= ![]() =
= ![]() = 4×105,反应正向进行的趋势很大 2H2O-4e-=O2↑+4H+ 40%
= 4×105,反应正向进行的趋势很大 2H2O-4e-=O2↑+4H+ 40%
【解析】
废旧锂电池材料含有钴酸锂(LiCoO2)、导电剂石墨和铝粉等,加草酸溶解,浸出液”的主要成分是LiHC2O4、Al(HC2O4),“浸出渣”的主要成分是CoC2O4,则生成CoC2O4的化学方程式为2LiCoO2+5H2C2O4=2LiHC2O4+2CoC2O4+4H2O+2CO2↑,H2C2O4用量过大时生成Co(HC2O4)2,然后加入碳酸钠发生CoC2O4+CO32-=CoCO3+C2O42-,分离出滤渣1为CoCO3,滤液1含草酸钠,滤渣1加盐酸溶解生成CoCl2,电解可得到Co,以此解答该题。
(1)LiCoO2中Li为+1价、O为-2价,则Co元素的化合价为+3价;
(2)“浸出”中生成CoC2O4的化学方程式为2LiCoO2+5H2C2O4=2LiHC2O4+2CoC2O4+4H2O+2CO2↑,若H2C2O4用量过大,CoC2O4与过量的H2C2O4反应转化成Co(HC2O4)2而溶解,导致CoC2O4的产率反而会降低;
(3)“转化”中加入Na2CO3溶液发生反应的离子方程式为CoC2O4(s)+CO32-(aq)CoCO3(s)+C2O42-(aq),该反应进行的程度较大,用平衡常数K解释原因为K=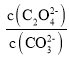 =
= ![]() =
= ![]() = 4×105,反应正向进行的趋势很大;
= 4×105,反应正向进行的趋势很大;
(4)由“电解”装置图可知,阳极的电极反应式为2H2O-4e-=O2↑+4H+,氢离子移向a,阴极区氯离子移向a,电解后a室中的电解液可返回酸溶工序继续使用;
(5)某废旧锂电池粉末中LiCoO2的质量分数为49%,将50吨该废料进行回收利用,电解得到钴5.9吨,则钴的回收率为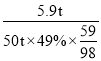 =40%。
=40%。

 名师导航单元期末冲刺100分系列答案
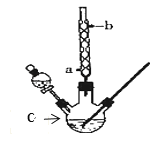
名师导航单元期末冲刺100分系列答案【题目】某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去)。已知下列数据:
乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 | |
熔点/℃ | ﹣117.3 | 16.6 | ﹣83.6 | |
沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
请回答下列问题:
(1)仪器C的名称为______,球形冷凝管的作用是_____。
(2)向C中加入反应物,待充分反应后,将C中的混合物倒入装有饱和碳酸钠溶液的烧杯中充分振荡洗涤。饱和碳酸钠溶液作用是(填字母):_____
A.中和乙酸并溶解乙醇
B.碳酸钠溶液呈碱性,有利于乙酸乙酯的水解
C.加速乙酸乙酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(3)经多次振荡洗涤、静置分液后,为了进一步提纯乙酸乙酯,可采用蒸馏的方法,蒸馏时控制温度在__左右,温度计的水银球应位于____。
(4)若实验所用乙酸质量为2.4g,乙醇质量为2.1g,得到纯净的产品质量为2.64g,则乙酸乙酯的产率是______。
(5)乙酸乙酯与氢氧化钠溶液发生反应的化学方程式为____________。