题目内容
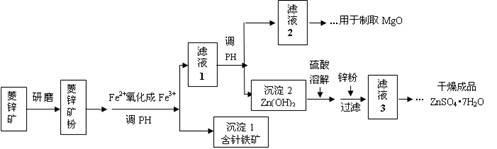
在实验室中,用锌、氧化铜、稀 为原料制取铜,有下列两种途径:①
为原料制取铜,有下列两种途径:①
②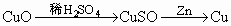
若用这两种方法制取铜的质量相等时,下列符合实验结果的是
[ ]
A.消耗相同质量的CuO
B.消耗相同质量的Zn
C.消耗相同质量的
D.生成硫酸锌的质量可能不同
答案:AD
解析:
解析:
|
据 Cu原子守恒,所需CuO的质量相等;由于前者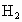 还原CuO时需先排空气,后在氢气中冷钾,故前者消耗的Zn、 还原CuO时需先排空气,后在氢气中冷钾,故前者消耗的Zn、 多,生成的 多,生成的 前者多. 前者多. |

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目