题目内容
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等。过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量。
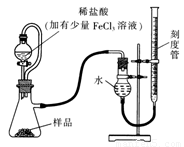
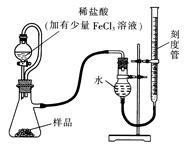
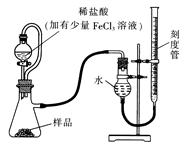
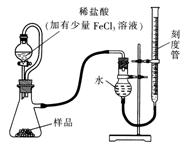
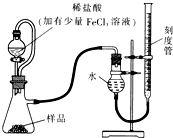
(1)某研究小组拟用右图装置测定一定质量的样品中过氧化镁的含量。
①实验前需进行的操作是 .稀盐酸中加入少量FeCl3溶液的作用是 。
②用恒压分液漏斗的优点有:使分液漏斗中的溶液顺利滴下; 。
③实验终了时,待恢复至室温,先 ,再平视刻度线读数。
(2)实验室还可通过下列两种方案测定样品中过氧化镁的含量:
方案I:取a g样品,加入足量稀盐酸,充分反应后再加入 NaOH溶液至Mg2+沉淀完全,过滤、洗涤后,将滤渣充分灼烧,最终得到b g固体。
方案Ⅱ:称取0.1 g样品置于碘量瓶中,加入15 mL0.6 mol/LKI溶液和足量盐酸,摇匀后在暗处静置5 min,然后用0.1 mol/L Na2S2O3溶液滴定,滴定到终点时共消耗VmL Na2S2O3溶液。(已知:I2+2Na2S2O3= Na2S4O6+2NaI)
①已知常温下Ksp[Mg(OH)2]=l×10-11。为使方案I中Mg2+完全沉淀[即溶液中c(Mg2+)≤l ×10-5mol/L],溶液的pH至少应调至 。方案I中过氧化镁的质量分数为 (用含a、b的表达式表示)。
②方案Ⅱ中滴定前需加入少量 作指示剂;样品中过氧化镁的质量分数为 (用含V的表达式表示)。
(1)①检查装置的气密性 用作催化剂(或催化H2O2的分解)
②消除滴入溶液的体积对所测气体体积的影响
③将右侧刻度管缓缓向下移动直到两侧液面相平
(2)④11 7(a-b)/2a
②淀粉溶液 2.8 V% ’
(第(2)②第一空1分,其余每空2分,本题共15分)
【解析】
试题分析:(1)①该实验是测量气体体积的装置,故实验前要检查装置的气密性;②用恒压分液漏斗的优点为使分液漏斗中的溶液顺利滴下和消除滴入溶液的体积对所测气体体积的影响;③气体的体积受到温度和压强的影响,故读数前要恢复至室温和恢复到常压,即将右侧刻度管缓缓向下移动直到两侧液面相平;(2)①根据前后物质的变化确定质量减少的是氧原子,n(O)=(a-b)/16mol=n(CuO2),过氧化镁的质量分数为②(a-b)/16×56÷a=7(a-b)/2a;②碘参与或生成的反应均采用淀粉溶液做指示剂;方案Ⅱ涉及的反应为
MgO2+2HCl=MgCl2+H2O2
2HCl+H2O2+2KI=2H2O+I2
I2+2Na2S2O3= Na2S4O6+2NaI
所以n(MgO2)=1/2n(Na2S2O3)=0.05×V×10-3mol
样品中过氧化镁的质量分数为=0.05×V×10-3×56/0.1=0.028V
考点:考查物质含量测定中实验操作、条件控制、数据分析等有关问题。

 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.