题目内容
在一定体积的密闭容器中,进行如下化学反应:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:
2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:
请回答下列问题:
(1)该反应的化学平衡常数表达式K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选项,多选不得分)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(CO)=υ逆(CO2) d.c(CO2)=c(CO)
(4)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。求该时间范围内反应的平均反应速率
υ(CO)= ,CO的平衡转化率为: 。
Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:
2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:| t℃ | 1000 | 1150 | 1300 |
| K | 64.0 | 50.7 | 42.9 |
请回答下列问题:
(1)该反应的化学平衡常数表达式K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选项,多选不得分)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(CO)=υ逆(CO2) d.c(CO2)=c(CO)
(4)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。求该时间范围内反应的平均反应速率
υ(CO)= ,CO的平衡转化率为: 。
(1)k=c(CO2)3/c(CO)3;(2)放热反应 (3)b、c (4)0.006 mol?L-1?min-1 60%
试题分析:(1)可逆反应Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g)的化学平衡常数表达式k=c(CO2)3/c(CO)3;(2)由表中数据可知,温度越高化学平衡常数越小,升高温度平衡向逆反应移动,正反应是放热反应;(3)a.无论反应是否达到平衡,该反应的压强均不变 ,故不能说明到达平衡状态,故a错误;
2Fe(s)+3CO2(g)的化学平衡常数表达式k=c(CO2)3/c(CO)3;(2)由表中数据可知,温度越高化学平衡常数越小,升高温度平衡向逆反应移动,正反应是放热反应;(3)a.无论反应是否达到平衡,该反应的压强均不变 ,故不能说明到达平衡状态,故a错误;b.反应达到平衡状态时,各物质的浓度不变,混合气体中c(CO)不变说明到达平衡状态,故b正确;
c.v (H2)正="v" (H2O)逆不同物质表示的速率之比等于化学计量数之比,说明到达平衡状态,故c正确;d.反应始终按CO与CO2物质的量之比为1:1进行,c(H2)=c(CO)不能说明到达平衡,故d错误;令平衡时CO的物质的量变化为nmol,则:
Fe2O3(s)+3CO(g)?2 Fe(s)+3CO2(g)
开始(mol):1 1
变化(mol):n 1+n
平衡(mol):1-n 1+n
所以[(1+n)/V]/[(1?n )V]=4,解得n=0.6,所以n(CO2)="0.6mol/10L/10min=0.006" mol?L-1?min-1,CO的平衡转化率为0.6mol 1mol×100%=60%。

练习册系列答案
相关题目
 2/3Fe(s) + CO2(g)
2/3Fe(s) + CO2(g)
 2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是( )
2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是( )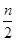 )
)


 2Z(g)、②2M(g)
2Z(g)、②2M(g)  N(g)+P(g)分别在密闭容器的两个反应室中进行, 反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行, 反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示: 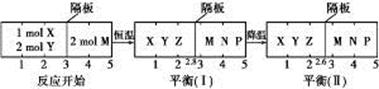

 cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的ΔH和ΔS判断正确的是( )
cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的ΔH和ΔS判断正确的是( )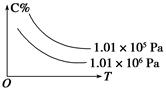
 CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1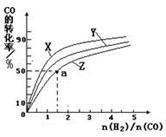
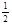 O2(g)=CO2(g) △H2=-283 kJ·mol-1 H2(g)+
O2(g)=CO2(g) △H2=-283 kJ·mol-1 H2(g)+ 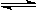 2C(g)+3D(g),达到平衡的标志是
2C(g)+3D(g),达到平衡的标志是