题目内容
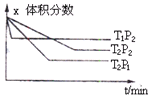
反应aX(g) + bY(g)  cZ(g);△H=Q,有下图所示关系,下列判断中正确是( )
cZ(g);△H=Q,有下图所示关系,下列判断中正确是( )
 cZ(g);△H=Q,有下图所示关系,下列判断中正确是( )
cZ(g);△H=Q,有下图所示关系,下列判断中正确是( )
| A.a+b < c, Q > 0 | B.a+b < c, Q < 0 |
| C.a+b > c, Q > 0 | D.a+b > c, Q < 0 |
D
试题分析:观察图可知,P1>P2,T1>T2。如果a+b<c,升高温度和增大压强化学平衡都逆向移动,图像不符合,故A、B项错误。如果a+b > c,根据图像,升高温度,X的量增多,正反应为放热反应,Q < 0,故选D。
点评:本题考查的是化学平衡移动的相关知识,题目难度中等,分析透彻影响化学平衡移动的因素是解题的关键。

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
 cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中不正确的是
cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中不正确的是 CH3OH(g)
CH3OH(g) 
 N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( ) CH3OH(g)
CH3OH(g)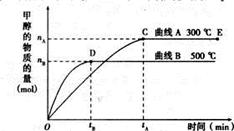
 CO(NH2)2(l) + H2O (l) ΔH < 0 。回答下列问题:
CO(NH2)2(l) + H2O (l) ΔH < 0 。回答下列问题: NH2COONH4(s) ΔH1< 0
NH2COONH4(s) ΔH1< 0 CO(NH2)2(l)+ H2O (l) ΔH 2> 0
CO(NH2)2(l)+ H2O (l) ΔH 2> 0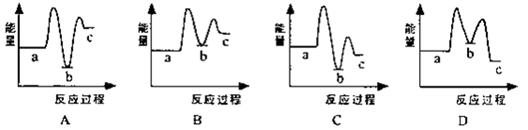
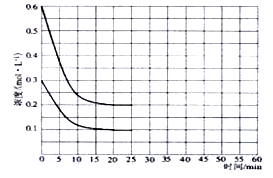
 2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
2HI(g)的K=50,由此推测在450℃时,反应2HI(g)  N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数 ( )
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数 ( ) 4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。