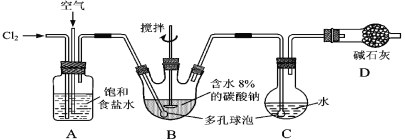
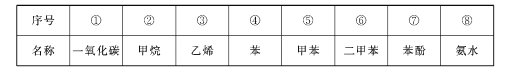
题目内容
【题目】在恒容密闭容器中通入物质的量浓度均0.1mol·L-1的CH4与CO2,在一定条件下发生反应:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图5,下列有关说法正确的是( )
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图5,下列有关说法正确的是( )

A. 上述反应的△H>0 B. 压强P1>P2>P3>P4
C. 1100℃该反应的平衡常数为64 D. 压强为P4时,在Y点:v(正)<v(逆)
【答案】A
【解析】A项,温度越高,转化率越大,升温平衡右移,ΔH>0,正确;B项,增大压强,平衡左移,CH4的转化率减小,所以p4>p3>p2>p1,错误;
C项, CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
起始/mol·L-10.1 0.1 0 0
平衡/mol·L-10.1-x 0.1-x 2x 2x
![]() ×100%=80% x=0.08
×100%=80% x=0.08
K=![]() =1.638 4,错误;D项,Y点未达平衡,若要达平衡,CH4的转化率应增大,所以v(正)>v(逆)。
=1.638 4,错误;D项,Y点未达平衡,若要达平衡,CH4的转化率应增大,所以v(正)>v(逆)。

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是_________________。非金属性最强的元素的原子结构示意图为__________________。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是________________________。
(3)②③④形成的简单离子半径由大到小的顺序是__________________________。
(4)元素⑦的氢化物分子式为_______________,该氢化物常温下和元素②的单质反应的离子方程式是____________________________________________。
(5)⑨的最高价氧化物对应的水化物化学式为__________________。①和⑨两元素形成化合物的电子式为___________________。
(6)①、⑥和⑦形成的化合物的化学式为__________________。该化合物的化学键类型为___________________________。
(7)⑧⑨三种元素形成的气态氢化物最稳定的是____________,沸点最高的是______________。
(8)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为____________________________。
(9)下列可以判断①和⑤金属性强弱的是____________________________。
a. ①单质的熔点比⑤单质低
b. ①质软,氧化物种类比⑤多
c. ①单质与水反应,⑤单质几乎不与水反应
d. ①最高价氧化物的水化物的碱性比⑤强