题目内容
2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g) 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=0.2 mol·L-1·s-1 B.z=3 C.B的转化率为25% D.C的体积分数为28.6%
【答案】
D
【解析】A的转化率为50%,则消耗A是1mol,则消耗B是1.5mol,生成C、D分别是1mol和z/2mol。所以B的转化率是1.5÷2×100%=75%,C不正确。又因为v(D)=0.25 mol·L-1·s-1,所以0.25 mol·L-1·s-1×2L×2s=z/2mol,解得z=2,B不正确。因为式量之比是相应的化学计量数之比,所以v(C)=v(D)=0.25 mol·L-1·s-1,A不正确,C的体积分数为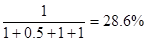 ,答案选D。
,答案选D。

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
 3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是 ( )
3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是 ( )  2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白。
2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白。