题目内容
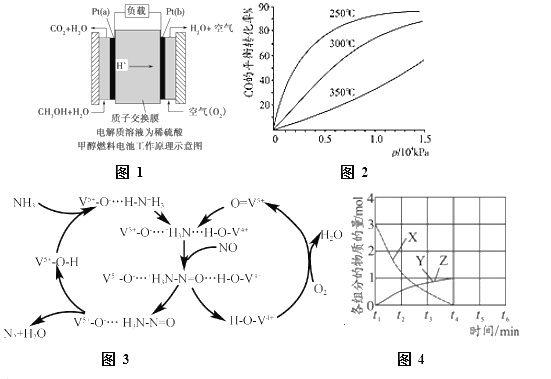
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700—900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是

A. 电池总反应为N2H4+2O2=2NO+2H2O
B. 电池内的O2-由电极乙移向电极甲
C. 电极乙上反应的电极方程式为:O2+2e-=O2-
D. 电池外电路的电子由电极乙移向电极甲
【答案】B
【解析】
该燃料电池中,负极上燃料失电子发生氧化反应,电极反应式为: N2H4+2O2--4e-=N2↑+2H2O,正极上氧气得电子发生还原反应,电极反应式为:O2+4e-=2O2-,电池总反应为:N2H4+O2=N2↑+2H2O。
A.反应生成物均为无毒无害的物质,负极上反应生成氮气,则电池总反应为:N2H4+O2=N2↑+2H2O,故A错误;
B.由上述分析可知电极甲为负极,电极乙为正极。放电时,阴离子向负极移动,即O2-由电极乙移向电极甲,故B正确;
C.电极乙上反应的电极方程式为:O2+4e-=2O2-,故C错误;
D.电池外电路的电子由负极移向正极,所以由电极甲移向电极乙,故D错误。答案选B。

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
【题目】下列实验能达到相应实验目的的是
选 项 | 试剂 | 实验目的 | 实验装置 | ||
X | Y | Z | |||
A | Na2SO3 | 稀HNO3 | 品红溶液 | 证明SO2具有漂白性 |
|
B | MnO2 | 浓盐酸 | KI-淀粉溶液 | 比较Cl2与I2的氧化性强弱 | |
C | Na2CO3 | 醋酸 | Na2SiO3溶液 | 证明酸性: CH3COOH > H2CO3 >H2SiO3 | |
D | 蔗糖 | 浓硫酸 | 溴水 | 证明浓硫酸具有脱水性、氧化性 | |
A. AB. BC. CD. D