题目内容
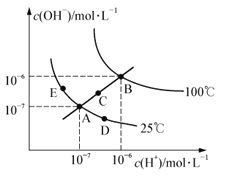
【题目】将浓度为0.1mol/L=HF溶液加水不断稀释,下列各量始终保持增大的是
A. c(H+) B. Ka(HF) C. ![]() D.
D. ![]()
【答案】D
【解析】试题分析:A、因HF为弱酸,则浓度为0.1molL-1HF溶液加水不断稀释,促进电离,平衡正向移动,电离程度增大,n(H+)增大,但c(H+)不断减小,A项错误;B、因电离平衡常数只与温度有关,则Ka(HF)在稀释过程中不变,B项错误;C、因稀释时一段时间电离产生等量的H+和F-,溶液的体积相同,则两种离子的浓度的比值不变,但随着稀释的不断进行,c(H+)不会超过10-7molL-1,c(F-)不断减小,则比值变小,C项错误;D、因Ka(HF)= c(F-)×c(H+)/ c(HF),当HF溶液加水不断稀释,促进电离,c(F-)不断减小,Ka(HF)不变,则c(H+)/ c(HF)增大,D项正确;答案选D。

【题目】根据所学知识回答下列问题
(1)以K、Na、H、O、S、N中任两种或三种元素组成合适物质,分别填在表中②、④、⑥后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①H2SO4 ②_______ | ③NaOH ④_______ | ⑤Na2SO4 ⑥_______ | ⑦CO2 ⑧SO3 | ⑨NH3 |
(2)写出①与少量的③溶液反应的离子方程式__________________________。
(3)写出铁与①溶液反应的化学方程式________________________________。
(4)某同学欲用10mol·L-1浓硫酸配制480 mL 1 mol·L-1的稀硫酸。配制480mL 1mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为_________mL。
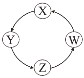
【题目】下列各组物质中,满足表中图示物质在一定条件下一步转化关系的组合有
序号 | X | Y | Z | W |
|
① | Si | Na2SiO3 | H2SiO3 | SiO2 | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①②③ B. ①③④ C. ②③ D. ①④