题目内容
【题目】CuSO4溶液是中学化学及农业生产中常见的一种试剂。
(1)某同学配制CuSO4溶液时,需加入一定量的硫酸溶液,用离子方程式说明其原因是___________。
(2)该同学利用制得的CuSO4溶液,进行以下实验探究。
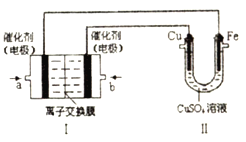
如图,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则a处电极上发生的电极反应式是___________。若只把Ⅱ中电极均换为惰性电极,电解时的化学反应方程式为___________。若把Ⅱ中电极均换为惰性电极,电解液换为含有0.04mol CuSO4和0.04mol NaCl的混合溶液400mL,当阳极产生的气体为672mL(标准状况下)时,溶液的pH=___________(假设电解后溶液体积不变)。
【答案】 Cu2++2H2O![]() Cu(OH)2+2H+ CH4-8e-+10OH-=CO32-+7H2O 2CuSO4+2H2O
Cu(OH)2+2H+ CH4-8e-+10OH-=CO32-+7H2O 2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 1
2Cu+O2↑+2H2SO4 1
【解析】(1)硫酸中氢离子抑制铜离子水解。
(2) 实现铁上镀铜,Cu为阳极,则b为正极,a为负极,甲烷失去电子,在碱性环境下生成碳酸根离子。把Ⅱ中电极均换为惰性电极,电极硫酸铜生成Cu、氧气、硫酸;根据电解方程式:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 ;2NaCl+2H2O
2Cu+O2↑+2H2SO4 ;2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;阳极生成的气体为氧气、氯气,结合离子的放电顺序可以知道,先生成氯气,结合电子守恒来计算。
2NaOH+H2↑+Cl2↑;阳极生成的气体为氧气、氯气,结合离子的放电顺序可以知道,先生成氯气,结合电子守恒来计算。
(1) CuSO4属于强酸弱碱盐,发生Cu2++2H2O![]() Cu(OH)2+2H+反应,水解显酸性,加入一定量的硫酸溶液,氢离子抑制铜离子的水解;正确答案:Cu2++2H2O
Cu(OH)2+2H+反应,水解显酸性,加入一定量的硫酸溶液,氢离子抑制铜离子的水解;正确答案:Cu2++2H2O![]() Cu(OH)2+2H+ 。
Cu(OH)2+2H+ 。
(2) 实现铁上镀铜,Cu为阳极,则b为正极,通入的气体氧气,a为负极,甲烷失去电子,电极反应为CH4-8e-+10OH-=CO32-+7H2O;把Ⅱ中电极均换为惰性电极,电解硫酸铜,阴极生成Cu、阳极生成氧气、硫酸,电解反应为2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 ;电解混合溶液时,阳极上氯离子放电,电极反应式为2Cl--2e-=Cl2↑,0.04mol氯离子只能生成0.02氯气,即448 mL氯气,转移0.04mol 电子,共生成672mL 气体,说明还有224 mL 气体来自于水的电解,根据4OH--4e-=O2↑+2H2O知,生成224 mL 氧气又转移0.04mol电子,所电解过程中一共转移0.08mol电子,阴极上先铜离子放电,电极反应式为Cu2++2e-= Cu,现有0.04mol铜离子恰好完全电解析出,由此可得整个过程中消耗了0.04mol 氢氧根离子,根据水的电离方程式知,溶液中氢离子浓度为0.04 mol ,则氢离子浓度为0.1mol/L,则溶液的pH=1;正确答案: CH4-8e-+10OH-=CO32-+7H2O;2CuSO4+2H2O
2Cu+O2↑+2H2SO4 ;电解混合溶液时,阳极上氯离子放电,电极反应式为2Cl--2e-=Cl2↑,0.04mol氯离子只能生成0.02氯气,即448 mL氯气,转移0.04mol 电子,共生成672mL 气体,说明还有224 mL 气体来自于水的电解,根据4OH--4e-=O2↑+2H2O知,生成224 mL 氧气又转移0.04mol电子,所电解过程中一共转移0.08mol电子,阴极上先铜离子放电,电极反应式为Cu2++2e-= Cu,现有0.04mol铜离子恰好完全电解析出,由此可得整个过程中消耗了0.04mol 氢氧根离子,根据水的电离方程式知,溶液中氢离子浓度为0.04 mol ,则氢离子浓度为0.1mol/L,则溶液的pH=1;正确答案: CH4-8e-+10OH-=CO32-+7H2O;2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 ;1。
2Cu+O2↑+2H2SO4 ;1。