题目内容
(6分)已知:MnO2+4HCl(浓)===MnCl2+Cl2↑+2H2O 一定质量的二氧化锰溶解在100mL过量的浓盐酸中,当反应生成4.48L氯气(标准状况)时,剩余溶液中盐酸的浓度为1mol/L(假设反应前后体积不变),求:
(1)反应耗用MnO2的质量
(2)被氧化的HCl的物质的量
(3)原浓盐酸的物质的量浓度
(1)反应耗用MnO2的质量
(2)被氧化的HCl的物质的量
(3)原浓盐酸的物质的量浓度
(6分)
(1)17.4g(2分) (2)0.4mol(2分)
(3)9mol/L(2分) (解题步骤根据本校的情况给分)
(1)17.4g(2分) (2)0.4mol(2分)
(3)9mol/L(2分) (解题步骤根据本校的情况给分)
略

练习册系列答案
相关题目
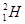 2O)中含NA个中子
2O)中含NA个中子 数为0.5NA
数为0.5NA