题目内容
近几年开发的甲醇燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:
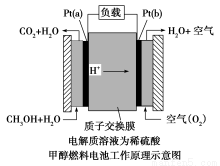
请回答下列问题:
(1)Pt(a)电极是电池的 极,电极反应式为 ;Pt(b)电极发生 反应(填“氧化”或“还原”),电极反应式为 。
(2)电池的总反应方程式为 。
(3)如果该电池工作时电路中通过2 mol电子,则消耗的CH3OH有 mol。
(1)负 2CH3OH+2H2O-12e-=2CO2↑+12H+ 3O2+12H++12e-=6H2O
(2)2CH3OH+3O2=2CO2+4H2O
(3)
【解析】从示意图中可以看出电极Pt(a)原料是CH3OH和水,反应后产物为CO2和H+,CH3OH中碳元素化合价为-2,CO2中碳元素化合价为+4,说明Pt(a)电极上CH3OH失去电子,电极Pt(a)是负极,则电极Pt(b)是正极,Pt(b)电极原料是O2和H+,反应后的产物为H2O,氧元素化合价由0→-2,发生还原反应,因为电解质溶液是稀H2SO4,可以写出电池总反应式为2CH3OH+3O2=2CO2+4H2O,再写出较为简单的正极反应式:3O2+12e-+12H+=6H2O,用总反应式减去正极反应式即可得到负极反应式为:2CH3OH+2H2O-12e-=2CO2↑+12H+。

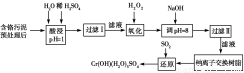
某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是
Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+)。
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 11.1 | 8 | 9(>9溶液) |
部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见上表。
(1)酸浸时,为了提高浸取率可采取的措施为________________(至少写一条)。
(2)调pH=8是为了除去________(填Fe3+、Al3+、Ca2+、Mg2+,下同)。
(3)钠离子交换树脂的原理为Mn++nNaR―→MRn+nNa+,被交换的杂质离子是________。
(4)试配平反应方程式:

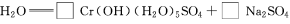 ;
;
生成1 mol Cr(OH)(H2O)5SO4消耗SO2的物质的量为________。
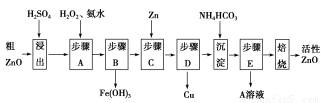
活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
已知:几种离子生成氢氧化物沉淀时的pH如表:
待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是 ,该步骤需控制溶液pH的范围是 。
(2)A溶液中主要含有的溶质是 。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS (选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为 mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。