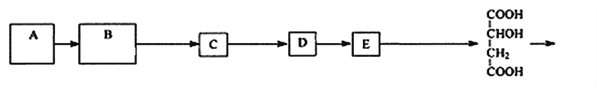
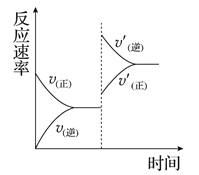
ƒøƒ⁄»ð
°æƒø°ø “Œ¬œ¬£¨œ¬¡–»Ð“∫÷–Œ¢¡£≈®∂»πÿœµ“ª∂®’˝»∑µƒ «
A. 0.1molLNa2CO3»Ð“∫£¨º”ÀÆœ° Õ£¨c(HCO3-)/c(CO32-)ºı–°
B. pH=7µƒ∞±ÀƔά»ªØ∞±µƒªÏ∫œ»Ð“∫÷–:c(Cl-)>c(NH4+)
C. 0.1molLµƒ¡ÚÀ·¬¡»Ð“∫÷–:c(SO42-)>c(Al3+)>c(H+)>c(OH-)
D. pH=2µƒ¥◊À·»Ð“∫∫ÕpH=12µƒNaOH»Ð“∫µ»Ãª˝ªÏ∫œ:c(Na+)=c(CH3COO-)+c(CH3COOH)
°æ¥∞∏°øC
°æΩ‚Œˆ°øA. Na2CO3»Ð“∫÷–¥Ê‘⁄úÀ·∏˘¿Î◊”µƒÀÆΩ‚∆Ω∫‚£¨CO32£≠£´H2O![]() HCO3£≠£´OH£≠£¨
HCO3£≠£´OH£≠£¨![]() =
=![]() £¨º”ÀÆœ° Õ£¨¥ŸΩ¯ÀÆΩ‚£¨»Ð“∫µƒºÓ–‘ºı»ı£¨µ´ÀÆΩ‚∆Ω∫‚≥£ ˝≤ª±‰£¨“Ú¥À
£¨º”ÀÆœ° Õ£¨¥ŸΩ¯ÀÆΩ‚£¨»Ð“∫µƒºÓ–‘ºı»ı£¨µ´ÀÆΩ‚∆Ω∫‚≥£ ˝≤ª±‰£¨“Ú¥À![]() ‘ˆ¥Û£¨π A¥ÌŒÛ£ªB£Æ∞±ÀƔά»ªØÔßµƒªÏ∫œ»Ð“∫¥Ê‘⁄µÁ∫… ÿ∫„£∫c(OH-)+c(Cl-)=c(NH4+)+c(H+)£¨ “Œ¬œ¬£¨ªÏ∫œ“∫pH=7£¨‘Úc(OH-)=c(H+)£¨À˘“‘c(Cl-)=c(NH4+)£¨π B¥ÌŒÛ£ªC.¡ÚÀ·¬¡»Ð“∫÷–¬¡¿Î◊”ÀÆΩ‚£¨»Ð“∫œ‘À·–‘£¨‘Úc(SO42-)>c(Al3+)>c(H+)>c(OH-)£¨π C’˝»∑£ªD.pH=2µƒ¥◊À·»Ð“∫÷–¥◊À·µƒ≈®∂»¥Û”⁄∫ÕpH=12µƒNaOH»Ð“∫£¨¥◊À·µƒ≈®∂»¥Û”⁄«‚—ıªØƒ∆µƒ≈®∂»£¨µ»Ãª˝ªÏ∫œ∫Û¥◊À·π˝¡ø£¨c(Na+)£ºc(CH3COO-)+c(CH3COOH)£¨π D¥ÌŒÛ£ªπ —°C°£
‘ˆ¥Û£¨π A¥ÌŒÛ£ªB£Æ∞±ÀƔά»ªØÔßµƒªÏ∫œ»Ð“∫¥Ê‘⁄µÁ∫… ÿ∫„£∫c(OH-)+c(Cl-)=c(NH4+)+c(H+)£¨ “Œ¬œ¬£¨ªÏ∫œ“∫pH=7£¨‘Úc(OH-)=c(H+)£¨À˘“‘c(Cl-)=c(NH4+)£¨π B¥ÌŒÛ£ªC.¡ÚÀ·¬¡»Ð“∫÷–¬¡¿Î◊”ÀÆΩ‚£¨»Ð“∫œ‘À·–‘£¨‘Úc(SO42-)>c(Al3+)>c(H+)>c(OH-)£¨π C’˝»∑£ªD.pH=2µƒ¥◊À·»Ð“∫÷–¥◊À·µƒ≈®∂»¥Û”⁄∫ÕpH=12µƒNaOH»Ð“∫£¨¥◊À·µƒ≈®∂»¥Û”⁄«‚—ıªØƒ∆µƒ≈®∂»£¨µ»Ãª˝ªÏ∫œ∫Û¥◊À·π˝¡ø£¨c(Na+)£ºc(CH3COO-)+c(CH3COOH)£¨π D¥ÌŒÛ£ªπ —°C°£