题目内容
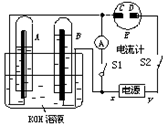
上海自主研发了一种氢燃料汽车。它是以30%KOH溶液为电解质的氢氧燃料电池,下列有关说法中,不正确的是
| A.正极反应:O2 + 2H2O + 4e- ="==" 4OH- |
| B.发生氧化反应的是负极 |
| C.当正极消耗22.4 L H2时,负极11.2 L O2消耗(相同条件) |
| D.氢氧燃料电池不仅能量转化率高,而且产物是水,属于环境友好电池 |
C
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。据此可知在氢氧燃料电池中氢气在负极通入,氧气在正极通入,所以选项C不正确,其余选项都是正确的,答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型与重要的考点。试题侧重对原电池原理的考查,以及灵活运用原电池原理解决实际问题的能力,有助于培养学生的应试能力,提高学习效率。该题的关键是明确原电池的原理,然后类推即可,有助于培养学生的逻辑推理能力。

练习册系列答案
相关题目
 CO32—+7H2O,下列叙述正确的是
CO32—+7H2O,下列叙述正确的是