题目内容
 铜是第四周期重要的过渡元素之一,其单质及化合物具有广泛用途.
铜是第四周期重要的过渡元素之一,其单质及化合物具有广泛用途.请回答下列有关问题:
(1)铜原子的基态电子排布式是
1s22s22p63s23p63d104s1或[Ar]3d104s1
1s22s22p63s23p63d104s1或[Ar]3d104s1
.比较第一电离能Cu<
<
Zn(填“>”、“=”、“<”),说明理由Cu失去1个电子后内层电子达到全充满的稳定状态
Cu失去1个电子后内层电子达到全充满的稳定状态
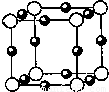
.(2)氮和铜形成某种化合物的晶胞结构如图所示,则其化学式为
Cu3N
Cu3N
.(每个球均表示1个原子)(3)铜可以形成多种多样的配合物.
①NH3可以和很多过渡金属形成配合物.NH3分子中心原子的杂化类型为
sp3
sp3
杂化,与NH3互为等电子体的粒子有H3O+
H3O+
.(只写其中一种)②向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.试用离子方程式表示其原因
Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+
Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+
、Cu(OH)2+4NH3=Cu(NH3)42++2OH-
Cu(OH)2+4NH3=Cu(NH3)42++2OH-
.(4)在绿色植物标本的制作过程中,将植物材料洗净后浸入5%的硫酸铜溶液中,叶绿素(如图1)中心离子Mg2+被置换成Cu2+(如图2),叶片则永保绿色,请在图2中用箭头表示出配位键.

分析:(1)铜的原子序数是29,同一周期元素的第一电离能随着原子序数的增大而增大;
(2)根据晶胞中微粒个数的分配方法计算化学式;
(3)①NH3分子中N原子呈3个N-H键,N原子还原1对孤对电子对,杂化轨道数为4,据此判断杂化方式;原子数和电子数目相同的微粒为等电子体;
②氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液;
(4)配位键是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态.
(2)根据晶胞中微粒个数的分配方法计算化学式;
(3)①NH3分子中N原子呈3个N-H键,N原子还原1对孤对电子对,杂化轨道数为4,据此判断杂化方式;原子数和电子数目相同的微粒为等电子体;
②氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液;
(4)配位键是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态.
解答:解:(1)铜原子的基态电子排布式:1s22s22p63s23p63d104s1;Cu失去1个电子后内层电子达到全充满的稳定状态,铜的第一电离能小于锌,
故答案为:1s22s22p63s23p63d104s1 或[Ar]3d104s1;<;Cu失去1个电子后内层电子达到全充满的稳定状态;
(2)根据晶胞中微粒个数的分配方法计算,晶胞中含有N原子的数目为8×
=1,Cu原子的数目为:12×
=3,故化学式为Cu3N,故答案为:Cu3N;
(3)①NH3分子中N原子呈3个N-H键,N原子还原1对孤对电子对,杂化轨道数为4,N原子采取sp3杂化;NH3的等电子体H3O+,故答案为:sp3;H3O+;
②氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+;Cu(OH)2+4NH3=Cu(NH3)42++2OH-,故答案为:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+;Cu(OH)2+4NH3=Cu(NH3)42++2OH-;
(4)配位键是指成键双方一方提供空轨道一方提供孤对电子. N元素最外层有5个电子通过3个共用电子对就可以形成 8 电子稳定结构.所以Cu与4个氮形成共价健的氮原子中,有2条是配位键,氮原子提供电子,Cu提供空轨道,故答案为: .
.
故答案为:1s22s22p63s23p63d104s1 或[Ar]3d104s1;<;Cu失去1个电子后内层电子达到全充满的稳定状态;
(2)根据晶胞中微粒个数的分配方法计算,晶胞中含有N原子的数目为8×
| 1 |
| 8 |
| 1 |
| 4 |
(3)①NH3分子中N原子呈3个N-H键,N原子还原1对孤对电子对,杂化轨道数为4,N原子采取sp3杂化;NH3的等电子体H3O+,故答案为:sp3;H3O+;
②氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+;Cu(OH)2+4NH3=Cu(NH3)42++2OH-,故答案为:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+;Cu(OH)2+4NH3=Cu(NH3)42++2OH-;
(4)配位键是指成键双方一方提供空轨道一方提供孤对电子. N元素最外层有5个电子通过3个共用电子对就可以形成 8 电子稳定结构.所以Cu与4个氮形成共价健的氮原子中,有2条是配位键,氮原子提供电子,Cu提供空轨道,故答案为:
 .
.点评:本题考查原子核外电子排布、晶胞计算、配位键等,题目难度较大,注意配位键是指成键双方一方提供空轨道一方提供孤对电子.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目